Autre thème abordé : Ma greffe de cheveux FUT en image - résultats de 0 à 1 an et 5 mois !
N'hésitez pas à me contacter sur le forum https://www.hairrestorationnetwork.com (mon pseudo est arthurSam) : Cliquez ici pour m'envoyer un message !
(english version is here)
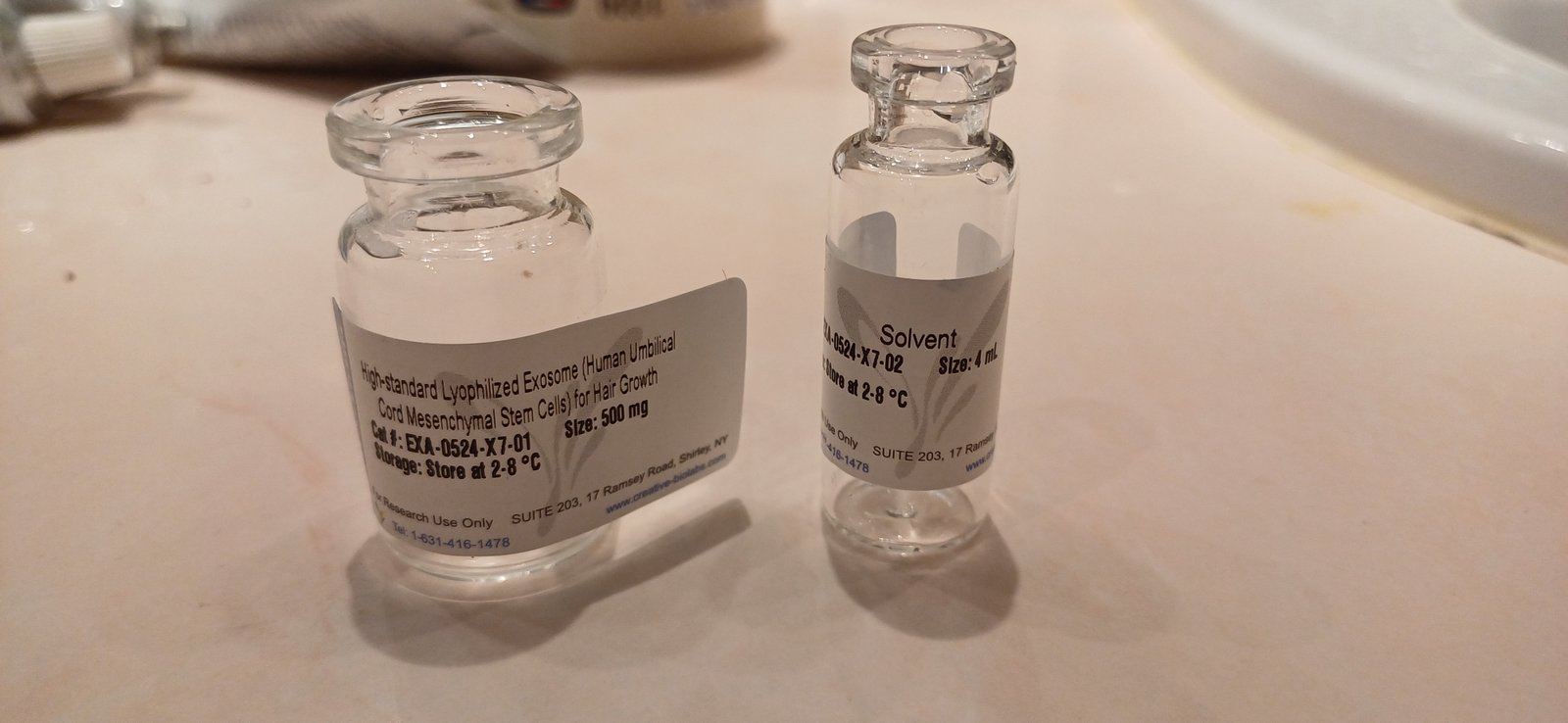
Je suis maintenant à ma 3ème bouteille de d'Exosomes Humains issus de cordon ombilical :

Juste après l'application des exosomes : les cheveux sont trempés par le produit:
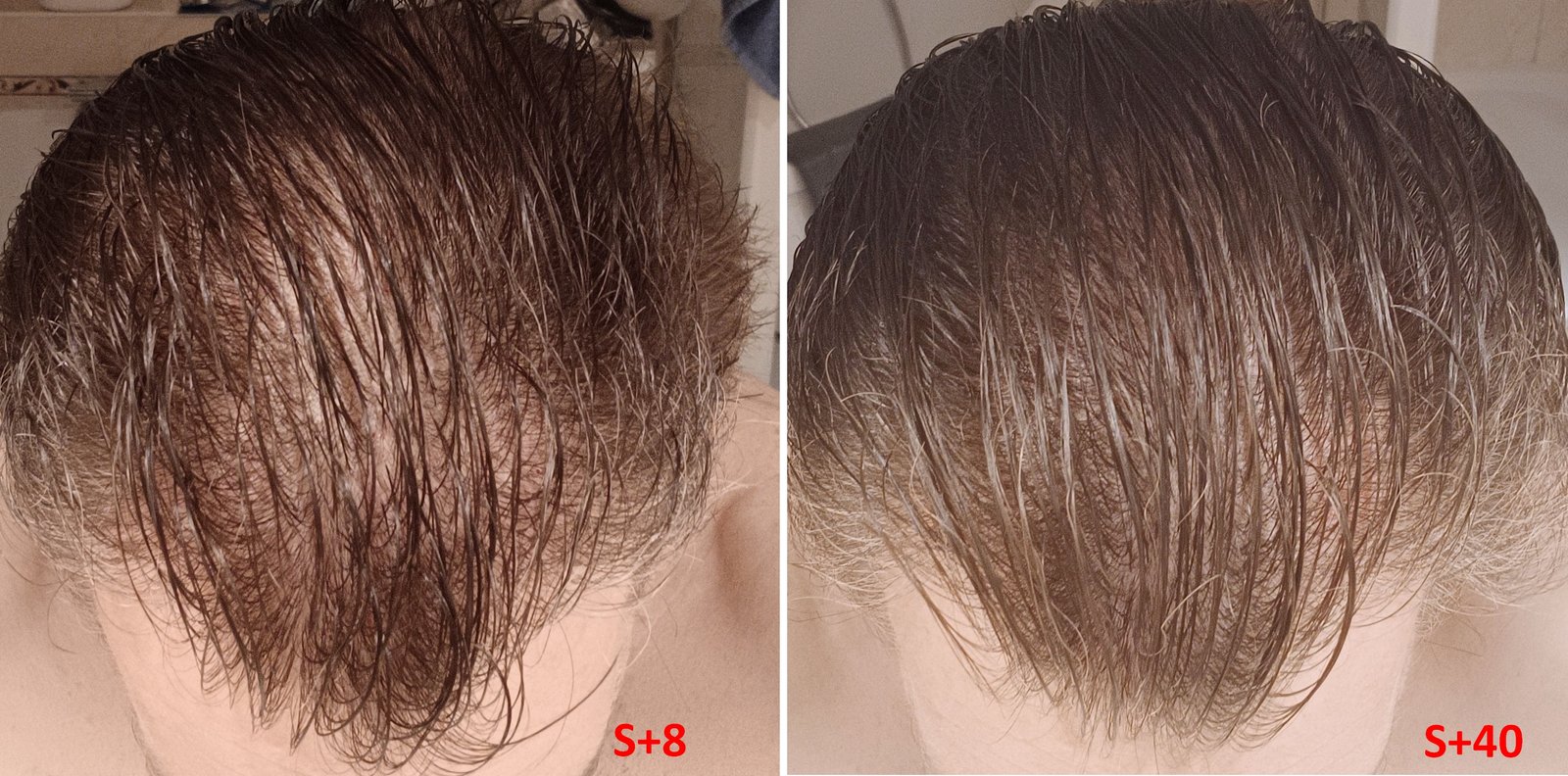
Mise à jour septembre 2024 :Je commence ma troisième bouteille d'exosomes humains issus de cordon ombilical. Je vais également maintenant utiliser Koshine826 (Pyrilutamide) à la place de CosmeRNA. En effet, après plus d'un an d'utilisation de CosmeRNA, les retours n'étant pas très glorieux, j'ai décidé d'utiliser Koshine826 qui est deux fois moins cher et qui ne sera pas pire que CosmeRNA !
Mise à jour mai 2024 : Comme mentionné dans le texte qui suit, le produit ASCE+ HRLV est basé sur des exosomes issues de plante (rose). Après 20 semaines de traitement, cela m'a apporté un peu de bénéfice mais rien d'extraordinaire ... je décide donc de changer de produit. Je passe maintenant aux produits suivants qui reposent sur des sources humaines :
Pour information, les AAPE ne sont pas des ASC-EXO (exosomes issues de cellules souches adipeuses) mais des ASC-CM (milieux conditionnés issus de cellules souches adipeuses), appelés sécrétomes.
L'ASC-CM est un cocktail complexe de protéines, d'acides nucléiques et de lipides libérés sous forme de facteurs solubles et/ou transportés dans des vésicules extracellulaires (EV). La différence entre les molécules du sécrétome réside principalement dans la taille de leurs particules. Les microvésicules sont plus grandes, environ 150 à 1 000 μm, tandis que les exosomes sont plus petites, environ 30 à 150 μm. Les exosomes pénètrent donc mieux dans la peau.
Sécrétome et exosomes sont parfois utilisés comme synonymes, mais ils sont en réalité différents.
Le sécrétome est l'ensemble de toutes les substances messagères libérées vers l'extérieur, y compris les micro-vésicules et les exosomes, mais aussi d'autres facteurs importants dissous dans le liquide. Il s'agit notamment de nombreux facteurs de croissance favorisant la régénération et de ce que l'on appelle les cytokines (messagers cellule-cellule).
Les exosomes, en revanche, ne sont en réalité que des exosomes particulaires isolés du tout. L'isolement les concentre, mais les solutés et micro-vésicules importants sont perdus.
A mon avis, les exosomes portent plus de microARN que de sécrétomes car elles sont davantage filtrées et peuvent donc stimuler par exemple la voie wnt/bêta-caténine qui est très importante pour la chute des cheveux.
Je vais donc continuer de prendre des exosomes, mais en ajoutant désormais également l'AAPE et faisant en sorte que les sources soient humaines et non issues de plantes. Je prends ce combo car je pense que les microARN sont importants en plus des diverses protéines / facteurs de croissances.
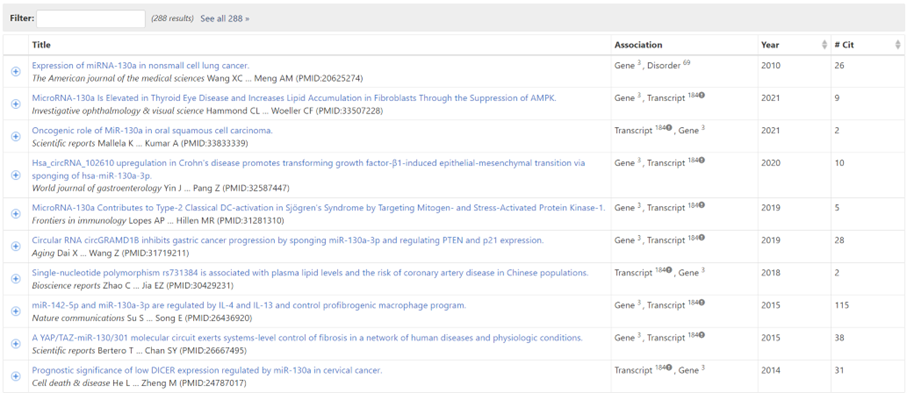
Vous trouverez la liste des micro-ARN que l'on trouve dans les exosomes issues des tissus adipeux et issues de cordon ombilical dans ce document de recherche. En les comparant avec les liste des micro-ARN qui ont un impact sur les cheveux (voir ce document de recherche), il semble qu'il y en ait davantage que dans les exosomes issues de la rose... ce qui est un bon point !
(Mise à jour 13 mars 2023 : ajout de deux vidéos sur les exosomes : "Extracellular vesicles characterization and therapeutic potential" & "Discussion and Q&A with the audience")
(Mise à jour 10 janvier 2023 : ajout des informations relatives au micro-ARN mir-122-5p contenu dans le produit ASCE+ HRLV)
(Mise à jour 28 avril 2024 : ajout des informations relatives au micro-ARN des exosomes de type ASC)
(english version is here)
.jpg)
L'étude qui est présentée dans la vidéo ci-dessus par le professeur Inigo DE FELIPE Y GARATE montre que l'ajout des exosomes ASCE+ HRLV à un traitement standard {Dutasteride 0.5mg/jour + Minoxidil oral 5mg/jour} apporte un bénéfice de 46% à l'efficacité du traitement sur 1 an ( C : group de controle sans exosomes / EXO : groupe avec les exosomes) :
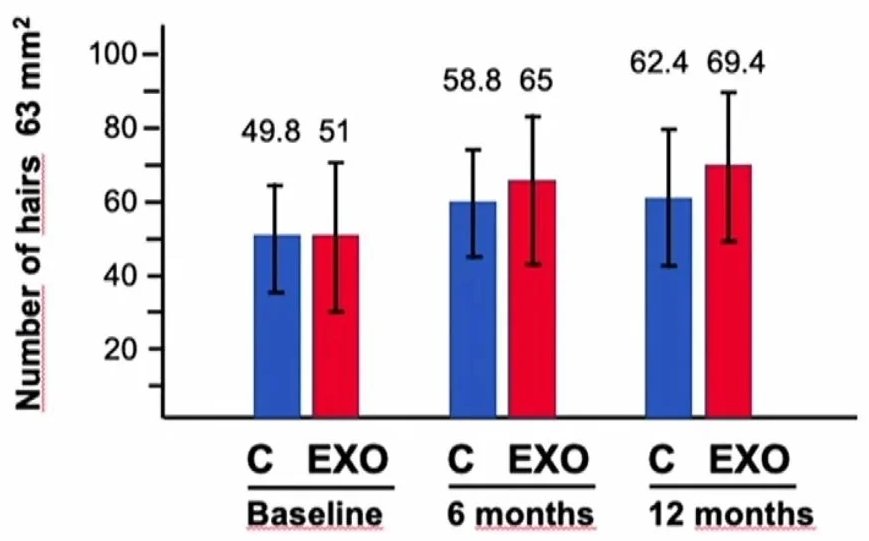
Je me suis donc lancé dans l'étude des exosomes afin de comprendre comment ils pourraient m'être utiles et je les prends maintenant depuis quelques semaines ...
Suite à ma greffe de 6500 cheveux FUT sans rasage (ce qui est équivalent à une FUE 3000 greffons - mon choix s'est porté sur la FUT car c'est ce type de greffe qui permet de maximiser les greffons et d'avoir des greffons les plus denses et solides et surtout le docteur pouvait me la faire sans rasage !) il y a maintenant plus d'un an faite par Paul Benet (voir ici les photos avec le pseudo EricLaurent - mon compte spécial greffe), je m’intéresse aux traitements pour lutter contre la progression de ma calvitie.
Comme j'avais encore quelques pertes de primitifs suite à ma greffe (une greffe n'arrête pas l'alopécie d'évoluer !), j'avais commencé par prendre du finastéride en topique 0.025%, 3 fois par semaine (en plus du minoxidil 5% que je prends depuis plusieurs dizaines d'années). Cela m'a permis d'arrêter ma chute mais j'ai dû mettre fin au traitement suite à l'apparition d'effets secondaire : douleurs au testicules, douleurs prostatiques, envies d'uriner fréquentes...
J'ai donc ensuite testé plusieurs médicaments en topique, dont le dutastéride à base de gel liposomal siliconé de type Xyon, que j'avais acheté à la pharmacie Parati (la constitution du gel Parati est la même que celle de Xyon). Cette formulation étant normalement sensée ne pas pénétrer dans le sang mais uniquement dans les follicules, j'étais plutôt confiant... mais malheureusement, là encore, j'ai eu des effets secondaires assez rapidement et j'ai dû arrêter mon traitement.
Malheureusement ces douleurs ne sont pas arrêtées tout de suite, mais continuent même un peu aujourd'hui ! C'est à ce moment que j'ai consulté le docteur Mousseigne pour avoir son avis et il m'a dit que j'avais un PFS (Post Finasterid Syndrome). Il m'a alors proposé de prendre un traitement interdit en France à base de stéroïdes mais que je pourrais trouver au Maroc. Si j'arrivais à récupérer les médicaments par l'intermédiaire de contacts de ce pays, il était prêt à m'aider à les doser et à les utiliser. J'ai toutefois préféré ne pas faire ces démarches car ce médicament est très dangereux.
Lors de cet entretien, il a également souhaité regarder ma greffe et il a beaucoup apprécié le travail de Monsieur Benet. Il m'a dit que ma greffe était très réussie :-)
Je suis bien sûr très satisfait de ma greffe, dont M. Mousseigne a dit qu'elle était très réussie.
Mais il faut penser au long terme et protéger ses cheveux, même après avoir été greffé !
J'ai donc commencé ensuite un traitement topique {Fluridil + CosmeRNA} en juin 2023 soit environ 1 an après ma greffe (7,5 mois au jour où j'écris ces lignes) pour lutter contre l'action de la DHT, et bien sûr en étant toujours sous minoxidil topique 5%. Ce traitement a freiné ma chute de cheveux et je n'ai aujourd'hui plus de primitifs qui tombent sous la douche !
C'est extrêment positif ! De plus, il semble que depuis ma prise de {CosmeRNA + Fluridil} des petits cheveux commencent à apparaître (voir mon post ici et ici et ici) ... j'espère donc maintenant les fortifier avec les exosomes ASCE+ HRLV de ExoCoBio.
Je me lance donc dans les exosomes en espérant gagner un peu en densité. Je n’ai plus de cheveux qui tombent et donc il semble que ma calvitie soit pour le moment stabilisée avec mon traitement.
Sur le forum international-hairlossforum.com, j'avais deux comptes : ArthurSam2 pour discuter des traitements contre la perte de cheveux, et EricLaurent pour discuter des résultats de ma greffe de cheveux.
J'avais choisi à l'époque d'utiliser deux pseudos différents car j'avais remarqué que tous les utilisateurs qui présentaient des résultats de greffes non faites par les docteurs belges ou par Mousseigne étaient systématiquement dénigrés.
J'avais également remarqué qu'ils sont très aggressifs envers les utilisateurs qui ont été gréffés avec des techniques autres que la FUE ... pourtant, de grandes cliniques réputées continuent de réaliser des FUT, comme par exemple Hattigen (voir cette vidéo par exemple) ! Dès lors que vous souhaitez une bonne densité en une seule session, c'est ce qui est conseillé si vous acceptez la cicatrice linéaire derrière la tête. Mais cette technique est beaucoup plus délicate que la FUE et demande une grande expérience que peu de docteurs continuent d'avoir...
J'avais d'ailleurs discuté de cela avec M. Bisanga à l'époque. Il m'avait dit alors que la FUT était une technique très efficace mais qu'avec le nombre croissant de demandes pour réaliser les FUE, il s'était davantage concentré sur les FUE et qu'il n'avait plus de personnel pour réaliser les FUT. Voici un extrait de sa réponse :
In terms of pricing, FUT requires twice the number of surgical team/techs than FUE and so is no longer the more economimcal opton. The reality of this, is that with FUE “leading” the market over FUT, clinics no longer require the same quantity of technicians as they once did as the vast majority of patients decide to proceed with FUE surgery. When FUT is scheduled, more technicians are required, meaning more expense to be covered, which will be absorbed into the cost of surgery for the patient, oftentimes meaning that FUT may now present a higher price than FUE, and is no longer the more economical option, which in turn results in FUT becoming even less attractive to many.
De plus, il y avait eu des problèmes judiciaires entre l'administrateur du forum et Paul Benet et je ne souhaitais donc pas être dénigré dès mon premier message concernant mes expériences sur les traitements de la perte de cheveux ! J'ai donc préféré mettre de l'anonymat entre ma greffe de cheveux et mes expériences sur les traitements.
Mais un utilisateur a finalement remarqué mon double compte et a commencé à me harceler sur le forum.
Tous les posts que j'ai créés sur le forum international-hairlossforum.com sont pollués par l'utilisateur Finn et ses compères qui me harcellent et qui m'ont forcé à être banni pour cause de ce double compte. Ces mecs sont des vrais collabos ne leur faite pas confiance !
Tous ces utilisateurs qui me harcèlent le font car ma greffe n'a pas été faite par leur greffeur "Mousseigne" et ils ne supportent pas la grande qualité de ma greffe, dont M. Mousseigne a justement dit qu'elle a très bien été réalisée (au moins, ce Monsieur est honnête ... pas comme tous ces utilisateurs qui me harcellent sur le forum ...).
Ces utilisateurs qui fréquentent le forum international-hairlossforum.com discréditent systématiquement tous ceux qui ne font pas de greffe avec Mousseigne
Ils sont certainement payés par ce Monsieur pour faire cela !
Ces utilisateurs ont commencé par écrire partout sur le forum international-hairlossforum.com que mes photos étaient volées ou truquées :

Ensuite, ces utilisateurs se sont même inscrits sur le forum international https://www.hairrestorationnetwork.com que je fréquente également pour discréditer et polluer tous mes message.
Finn et l'administrateur du forum international-hairlossforum.com ont même tenté de faire croire à l'administrateur du forum anglais que ma greffe a été faite par Mousseigne et non par Paul Benet, tout cela dans le but de me faire bannir :
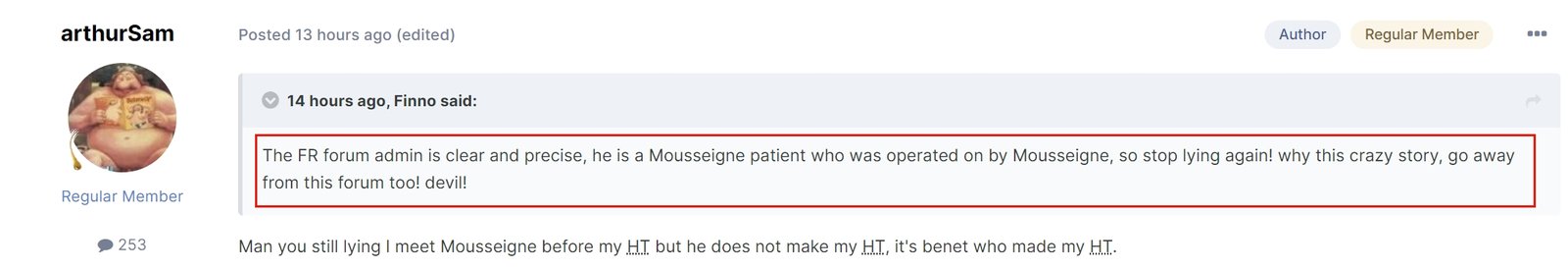
Vous pouvez ainsi voir que même l'administrateur du site international-hairlossforum.com participe à toute cette mascarade !
Ces mêmes utlilsateurs ont également envoyés des faux messages sur reddit, en accord avec l'administrateur du forum international-hairlossforum.com en volant mes photos publiées sur le forum hairrestorationnetwork.com et en les publiant avec des propos diffamatoires :

Vous voyez à quel point ces utilisteurs qui ont été gréffés par Mousseigne sont haineux et néfastes dès lors que vous ne passez pas par les même docteurs qu'eux !
Encore une fois, ils incitent les nouveaux arrivant sur le forum à se faire greffer par Mousseigne et ils sont certainement payés par ce Monsieur !
Finn poursuit même maintenant ses investigation chez les Allemand... :
Ce gros débile de Finn', qui ne sait même pas parler Français et doit avoir le QI d'une moule, s'est finalement fait remettre les points sur les "i" par l'administrateur du forum Anglais ! Au moins il n'aura pas réussi à le manipuler, comme il l'a fait sur le forum Français !
Aller, passons aux choses sérieuses !
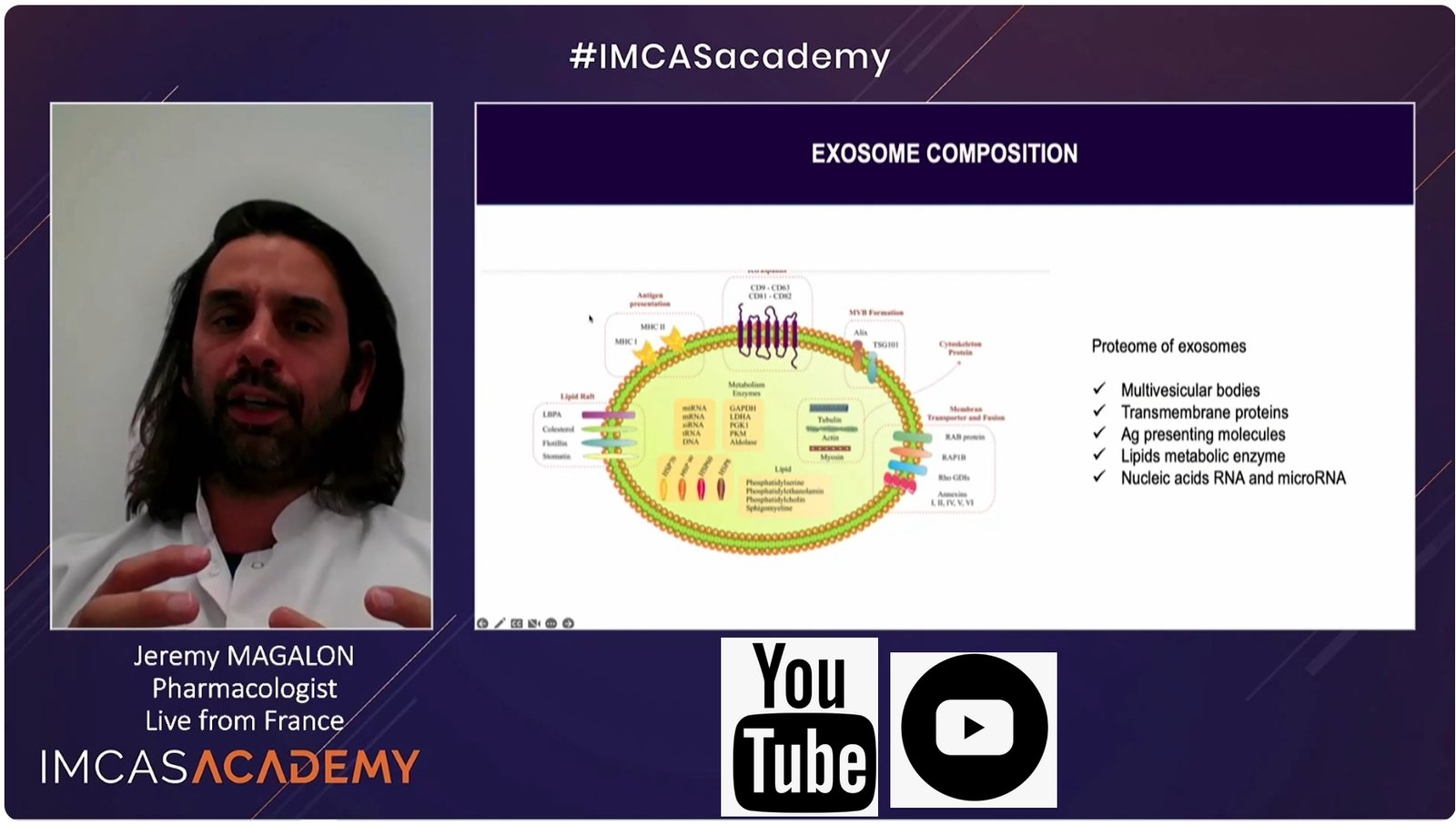 |
 |
| Extracellular vesicles characterization and therapeutic potential | Discussion and Q&A with the audience |
Voici donc un résumé de ce que j'ai pu lire sur ce domaine. Mon objectif était de comprendre ce que sont les exosomes et en quoi ils peuvent peut-être m'aider dans la lutte contre l’alopécie. J’ai voulu me faire une idée de l’efficacité que le produit ASCE+ HRLV (que j’ai choisi d’utiliser) peut avoir, et essayer de comprendre comment il peut apporter une amélioration de ma triste condition…
Le produit ASCE+ HRLV semble très répandu dans les cliniques et donc de bonne qualité. Il existe des exosomes beaucoup moins chères comme le Hanheal Hair mais j’ai de gros doutes sur la qualité de ce produit…
Vous allez voir qu’après avoir effectué des recherches afin de bien comprendre le rôle que peuvent avoir les exosomes sur l’alopécie, je suis malheureusement un peu partagé sur le produit ASCE+ HRLV au niveau de l’efficacité théorique qu’il pourrait avoir. Mais je me lance quand même car il semble y avoir de bons retours de dermatologues qui l’utilisent en mésothérapie… Et puis l’alopécie est un processus très complexe. N’étant pas médecin, j’aimerais également solliciter l’aide des membres de ce forum pour contredire, ou au contraire confirmer, mes idées et mes remarques.
La routine que j’ai prévu de suivre avec ces exosomes sera la suivante :
Pour la mésothérapie, j’utilise le mésogun dermajet 300 avec des aiguilles mutineedles 5-pins 1mm:
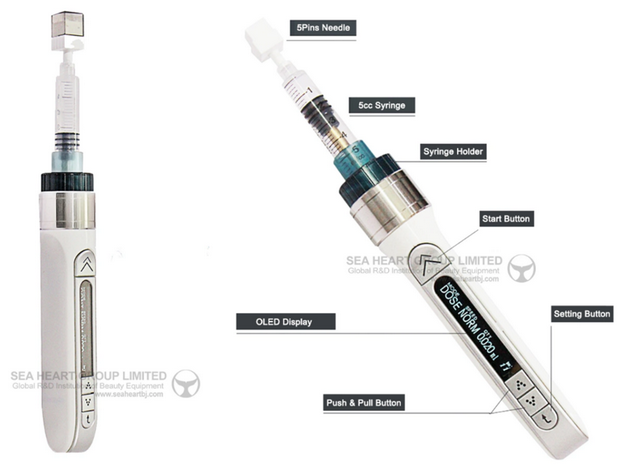

Procédure lors d’une séance :
Ne pas toucher au scalp dans les 4h qui suivent.
Ne rien appliquer, ni faire de shampoing ni sport pendant les 12h qui suivent.
Pour suivre les évolutions, je ciblerai des zones spécifiques de mon cuir chevelu et je posterai des images tous les mois.
Bien entendu, je ne poste ici que dans un but informatif, je ne sais pas si ce produit va fonctionner et donc je ne fais aucune préconisation sur son achat et son utilisation !
Sommaire :
Sources :
The AR/miR-221/IGF-1 pathway mediates the pathogenesis of androgenetic alopecia
Biological Function of Exosome-like Particles Isolated from Rose (Rosa Damascena) Stem Cell Culture Supernatant
Targeting Wnt/β-Catenin Pathway for Developing Therapies for Hair Loss
Dihydrotestosterone-Inducible Dickkopf 1 from Balding Dermal Papilla Cells Causes Apoptosis in Follicular Keratinocytes
Perspectives on miRNAs Targeting DKK1 for Developing Hair Regeneration Therapy
The Hair Follicle as a Dynamic Miniorgan
Mesenchymal Stem Cell-Derived Exosomes and MicroRNAs in Cartilage Regeneration: Biogenesis, Efficacy, miRNA Enrichment and Delivery
Mesenchymal Stem Cell-Derived Exosomes Promote Fracture Healing in a Mouse Model
Adipose Mesenchymal Stromal Cell-Derived Exosomes Carrying MiR-122-5p Antagonize the Inhibitory Effect of Dihydrotestosterone on Hair Follicles by Targeting the TGF-β1/SMAD3 Signaling Pathway
La version Anglaise est ici : https://www.hairrestorationnetwork.com/topic/71077-i-have-just-started-exosome-treatment-with-home-mesotherapy/
Bonne lecture !
Que sont les exosomes ?
La découverte des vésicules extracellulaires, ou exosomes, remonte aux années 1940. Les chercheurs ont commencé à s'y intéresser seulement à partir du milieu des années 2000 lorsqu'ils ont compris qu'ils permettent les échanges d'informations entre les cellules. Il y a eu plus de 3000 publications sur ce sujet dans les années 2018 et 2019… la course à la commercialisation des thérapies basées sur l'utilisation des exosomes est donc lancée. Les quatre principales start-ups dans ce domaine sont Codiak Biosciences, Exosome Diagnostics, Evox Therapeutics et ExoCoBio. Elles ont reçu plus de 385 millions de dollars d'investissement. Il y a eu également de nombreux accords qui se sont créés entre les start-ups et les grandes entreprises pharmaceutiques.
Les exosomes sont une classe de vésicules extracellulaires (EVs – Extracellular Vesicles) de taille nanométriques (30nm à 200nm), libérées par pratiquement toutes les cellules eucaryotiques (cellules qui ont un noyau lié à une membrane - les cellules de notre corps). Les exosomes peuvent être extraites de cellules souches et peuvent avoir de nombreuses applications thérapeutiques. Ces effets thérapeutiques résultent d'une forme particulière de la transmission de l'information entre les cellules : la signalisation paracrine. En effet, ces signaux émis par les cellules induisent des changements dans les cellules à proximité, ce qui altère leur comportement. Ces signaux sont transmis à faible distance, contrairement aux signaux transmis par le système endocrinien avec les hormones. Les chercheurs ont mis en évidence que les exosomes jouent un rôle très important dans les effets liés à la signalisation paracrine.
Une fois les exosomes extraits des cellules souches et purifiés, elles sont « chargées d’une cargaison ». Cette cargaison peut ensuite être transférée à d’autres cellules et donc modifier leur comportement cellulaire. On y trouve les matériaux suivants :
Les lipides jouent le rôle de stockage d’énergie dont les cellules de notre organisme ont besoin pour vivre.
Les protéines sont des macronutriments à la base de tout organisme vivant. Elles sont synthétisées dans la cellule au niveau du ribosome (qui se trouve à l’extérieur du noyau), à partir de l’information codée dans les gènes (l’ADN est stocké dans le noyau) qui détermine l’ordre dans lequel les acides aminés vont se séquencer. Des modifications post-transcriptionnelles peuvent intervenir une fois la protéine synthétisée, ce qui peut avoir pour effet d’en modifier les propriétés physiques ou chimiques.
De nombreuses protéines, résultant de l’expressions de gènes spécifiques, sont impliquées dans la régulation d’événements physiologiques au niveau de la peau et du cheveu. Nous reviendrons sur ce point lorsque nous étudierons comment se forment les cheveux.
Les ARN messagers sont des copies d’une région de l’ADN qui sont gardés à l’intérieur du noyau cellulaire. Puisque les ribosomes synthétisant les protéines sont à l’extérieur du noyau de la cellule, lorsqu’une cellule a besoin d’une protéine, l’ARN messager est exporté en dehors du noyau et rejoint les ribosomes où elle permet la synthèse de la protéine demandée.
Le taux de transcription d’une information génétique depuis l’ADN vers l’ARN messager est contrôlé par des protéines appelées des facteurs de transcription. Leur rôle est d’activer ou de désactiver des gènes afin qu’ils soient exprimés au bon moment et avec le bon taux dans les cellules désirées de l’organisme. Ces facteurs de transcription ont donc un rôle important dans la division cellulaire, la croissance des cellules et leur mort. Il y a 1500-1600 facteurs de transcription dans le génome humain. Ces facteurs de transcription peuvent travailler seuls ou accompagné de protéines.
Les ARN non codants correspondent à l’ensemble des ARN issus de la transcription de l’ADN mais qui ne seront pas traduits en protéines par la machinerie ribosomique. Ils interviennent toutefois à de nombreuses échelles dans la régulation de la synthèse protéique et/ou de la maturation des autres ARN. Parmi eux, on retrouve entre autres les micro-ARN (miARN).
Les micro-ARN sont donc des ARN non codants qui contrôlent l’expression génétique au niveau post-transcriptionnel. Les micro-ARN règlent l’expression génique en s’appariant avec des ARN messagers cibles dont ils sont partiellement complémentaires. Ils inhibent alors l’expression de leurs gènes cibles, provoquant le blocage de la traduction en protéine ou leur dégradation.
De nombreux miRNA ont été identifiés comme étant impliqués dans la régulation d’événements physiologiques au niveau de la peau et du cheveu, tels que la régulation de la différenciation des kératinocytes ou encore dans le mécanisme de sénescence. Certains ont même été identifiés comme étant impliqués dans le développement de pathologies cutanées telles que le psoriasis. Nous reviendrons en détails ce sur point par la suite.
Notons que dans la catégorie des ARN non codant on trouve également les petits ARN interférents (siRNA – Small Interfering RNA). Tout comme les miARN, ces petits ARN interférents sont capables de réguler les gènes car l’interférence avec un ARN messager spécifique conduit à sa dégradation et à la diminution de sa traduction en protéine.
Les exosomes extraites de cellules souches mésenchymateuse : Exosomes MSC
Les exosomes extraites de cellules souches mésenchymateuses (exosomes MSCs – Mesenchymal stem/stromal cells), présentent par exemple dans le mésenchyme (tissu) de l’embryon, le sang de cordon ombilical, la moelle osseuse ou le tissu adipeux, semblent les plus saines pour une utilisation thérapeutique. Ces exosomes MSCs peuvent par ailleurs être stérilisées alors que les cellules souches MSC ne le peuvent pas. Les exosomes MSCs sont considérées comme sans danger dans le domaine des traitements par cellules souches. Les exosomes MSCs ont été utilisées comme alternatives aux traitements par cellules souches MSCs dans de nombreux domaines : neurologiques, cardiovasculaires, système immunitaire, système rénal, musculosquelettique, hépatique, respiratoire, vision, maladies de la peau et cancers.
L’origine des exosomes MSC joue un rôle sur la qualité de l’effet thérapeutique
Les cellules souches MSC ont des propriétés de différentiations et d’auto-renouvellement par divisions cellulaires. Ces cellules souches peuvent être extraites depuis plusieurs types de tissus ou de liquides : tissu adipeux, moelle osseuse, pulpe dentaire, placenta, cordon ombilical, liquide synovial, liquide amniotique ou encore la gelée de Wharton.
Selon leur origine, les cellules souches MSC peuvent être différentiées en divers types de cellules comme les adipocytes (présentes dans les tissus adipeux), les chondrocytes (présentes dans le cartilage), les ostéoblastes (cellule osseuse jeune) et les myocytes (fibres musculaires). Les MSCs ont aussi des propriétés immunomodulatrices permettant de réguler différentes cellules jouant un rôle dans la réponse immunitaires. C’est la raison pour laquelle les MSCs ont été étudiées avec autant de ferveur au cours de ces dernières dizaine d’années.
Puisque les caractéristiques et les fonctionnalités des MSC varient en fonction de leur origine, il en résulte qu’il en est de même pour les exosomes qui en sont extraites. Des recherches ont montré par exemple que les exosomes issues des cellules souches du tissus adipeux (exosomes de type MSC-ASC) peuvent avoir un effet thérapeutique sur la maladie l’Alzheimer mais auraient des bénéfices contradictoires sur les cancers. L’origine des exosomes joue donc un rôle dans le type de maladie ciblée.
Le cycle des cheveux
Le cycle de vie des cheveux est un processus dynamique et complexe, composé d’une phase de croissance rapide qui dure pendant une longue période (phase anagène, d’une durée de 2 à 8 ans), une phase pendant laquelle les follicules régressent (phase catagène, d’une durée de 2 à 3 semaines) et une phase de repos (phase télogène, d’une durée d’environ 3 mois). Lors du re-déclenchement d’une nouvelle phase anagène, un nouveau follicule est créé et expulse l’ancien follicule (on parle aussi de phase exogène) :
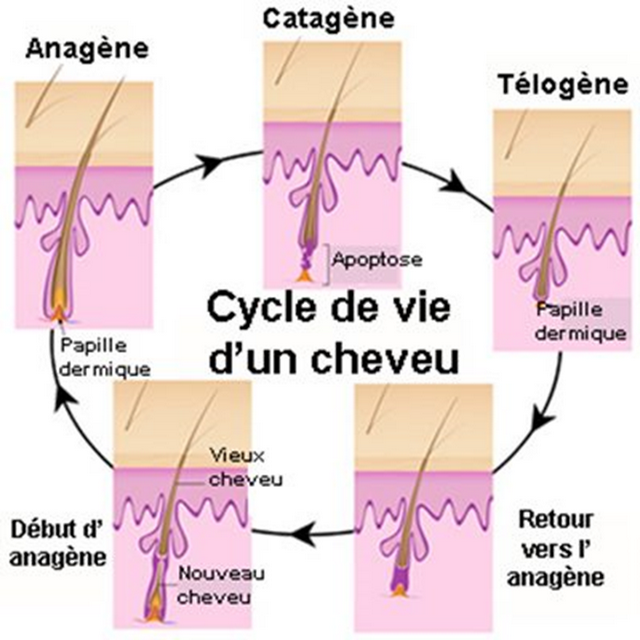
Anatomie des cheveux
Un follicule mature (anagène) peut être divisé en une partie supérieure visible et une partie inférieure qui est remodelée perpétuellement pendant les cycles. C’est dans la partie inférieure que se trouve l’usine qui gouverne la formation du cheveu, dans le bulbe. C’est ici que se trouvent la matrice cellulaire kératinocytes (composée de cellules amplifiées dérivées des cellules souches épithéliales des follicules) et l’unité de pigmentation du cheveu. Lorsque cette matrice est activée, les cellules prolifèrent et se différentient dans la région qui l’entoure. Leur nombre détermine alors la taille du bulbe et le diamètre du cheveu.
Lorsque les cellules de la matrice arrêtent de proliférer et de se différentier, elles auront engendré diverses lignées de cellules dans la tige du cheveu (hair shaft) et la gaine épithéliale interne (IRS – Inner Root Sheath). La gaine épithéliale externe (ORS – Outer Root Sheath) est quant à elle une extension de l’épiderme et elle contient un grand nombre de cellules qui jouent des rôles spécifiques sur la vie du follicule.
Dans le bulbe se trouvent également la papille dermique constituée de cellules mésenchymateuses appelées fibroblastes de la papille dermique. Les fibroblastes de la papille dermique génèrent des signaux dans la matrice provoquant la prolifération, la migration et la différenciation des cellules de cette matrice, essentielles à la croissance du follicule pileux. La papille dermique régule la taille du bulbe, le diamètre du cheveu et sa longueur ainsi que la durée de la phase anagène.
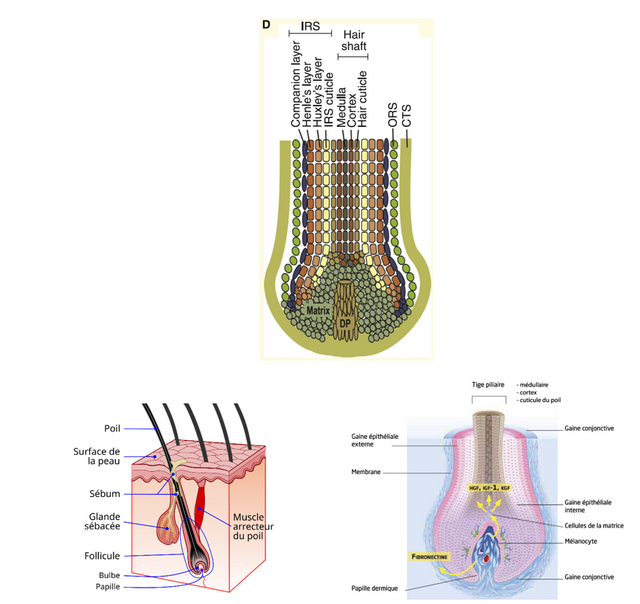
Développement embryonnaire des follicules
Le prérequis essentiel pour le développement d’un follicule est la communication moléculaire entre les cellules de l’épiderme et celles du tissu mésenchyme sous-jacent du derme. Ces communications sont organisées suivant des voies de transductions, et il en existe de plusieurs sortes. La transduction du signal est le mécanisme par lequel une cellule répond à l’information qu’elle reçoit, par des agents chimiques ou autres signaux (tension, …). Elle commande une cascade de signaux secondaires, internes à la cellule (« signalling ») ou externes (par exemple une action sur d'autres types cellulaires via des interleukines), et des processus cellulaires internes (métabolisme, cycle cellulaire, mortalité, ...).
La grande majorité des voies de transduction fait intervenir l’accrochage de molécules (appelées des ligands) sur des récepteurs de la cellule qui enclenchent des évènements à l’intérieur de la cellule. Parmi les molécules qui peuvent venir se fixer aux récepteurs, on trouve par exemple un grand nombre de facteurs de croissance (protéines qui régulent la fabrication ou la croissance de certaines cellules), de cytokines (substance secrétée par les cellules du système immunitaire pour qu’elles puissent communiquer entre elles), de neuropeptides (hormone ayant une fonction de neuromodulateur) et d’hormones (substance chimique élaborée par une glande et qui agissent sur le développement d’un organe), qui en partie sont produites par le follicule lui-même. Le follicule est donc très sensible à ces différentes molécules :
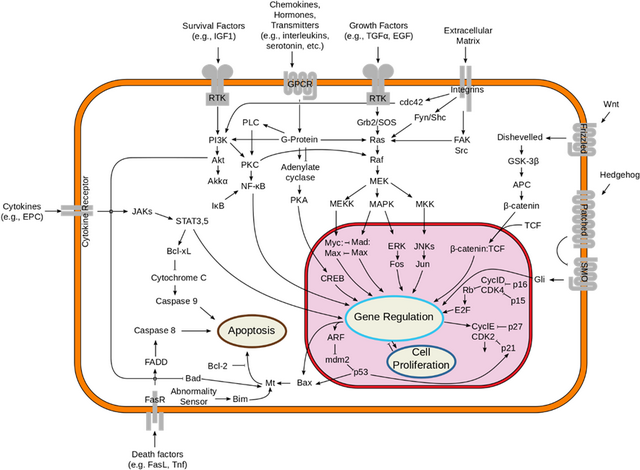
Parmi les molécules secrétées par les voies de transductions qui nous intéressent dans le cas de la communication entre les cellules de l’épiderme et celles du tissu mésenchyme du derme, on trouve les molécules intervenant dans les familles des voies de signalisations suivantes :
La formation d’un cheveu, qui intervient principalement pendant la vie embryonnaire, est induite par une combinaison spécifique de ces différents signaux. Elle comporte trois phases : l’induction, l’organogénèse et la cytodifférenciation.

La phase d’induction (étapes 0 et 1) :
Bien que le développement des cheveux intervient principalement pendant la vie embryonnaire, les voies de signalisations qui y sont mises en œuvre jouent également un rôle très important dans la régénération des cheveux chez l’adulte pendant leur cycle de vie. En effet, ces voies de signalisations régulent les interactions entre les cellules épithéliales et les cellules mésenchymateuses dans les follicules. On trouve par exemple les voies de hedgehog (via la protéine ssh), notch, TGF-beta et la voie Wnt.
Le cycle des follicules
Une fois la formation d’un premier follicule postnatal, il commence son cycle de vie :
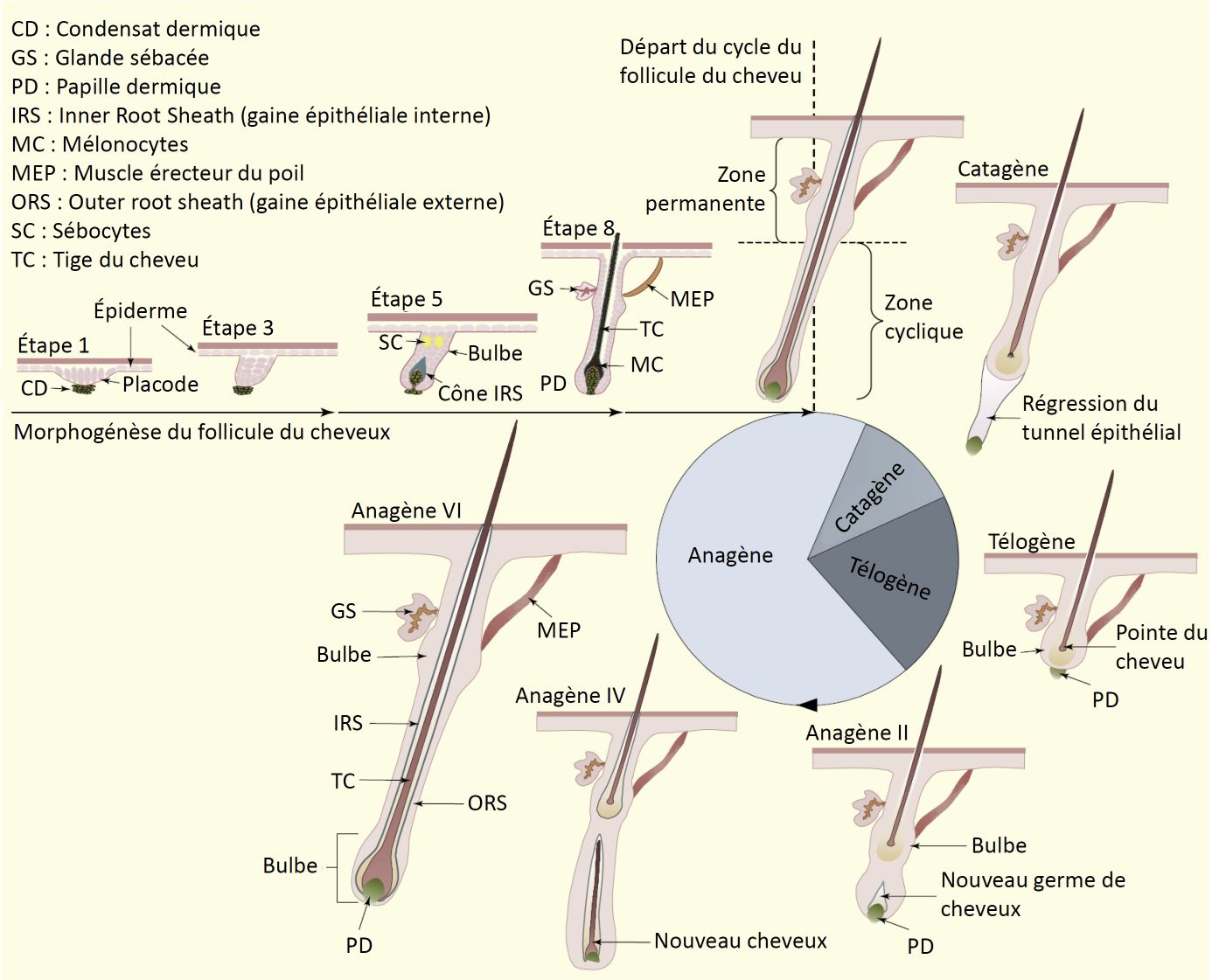
Pendant la phase anagène, la matrice kératinocytes résultante des cellules progénitrices (d’amplification transitoire) dérivées des cellules souches épithéliales de follicules contenues dans le bulbe, prolifèrent intensément et engendre de nombreuses cellules épithéliales. Cette prolifération est activée par les signaux engendrés depuis les cellules de la papille dermique.
Pendant la phase catagène, les deux-tiers de la base du follicule régresse principalement par apoptose (autodestruction) des cellules kératinocytes composant les couches externes du cheveu alors que les cellules souches contenues dans le bulbe échappent à l’apoptose. Il se produit également un rétrécissement du canal épithélial, ce qui a pour effet de séparer la papille dermique du bulbe.
Lorsque la phase catagène est terminée, les follicules entrent en dormance (phase télogène). Cette phase dure habituellement plus de 3 semaines et s’allonge avec l’âge. Durant cette phase, la papille dermique reste proche du bulbe, ce qui permet une très forte interaction entre les cellules souches contenues dans le bulbe et la papille dermique. La papille dermique joue un rôle essentiel pour l’activation des cellules souches et l’initialisation d’un nouveau cycle.
Bien qu’il ait de fortes corrélations entre les molécules qui vont participer au développement d’un follicule au stade embryonnaire et celles qui vont participer au renouvellement d’un follicule pendant le cycle de vie des cheveux, quelques différences existent. Par exemple, certains membres de la voie de signalisation TGF-beta et certains facteurs de croissance ont des fonctions opposées pendant le développement embryonnaire du follicule et son renouvellement : alors qu’ils stimulent leur développement embryonnaire, il stimule la phase catagène dans les follicules matures. D’autres signaux, comme ceux issus des voies de signalisations notch ou VDR (qui est contrôlée par la vitamine D), ne sont pas indispensables au développement du follicule mais le sont pour induire la phase anagène.
Certains mécanismes moléculaires qui dictent la dynamique de ces différentes phases sont connus. Par exemple, la phase anagène est activée par les Wnt/beta-caténine, les antagonistes des BMP et les Shh. Cependant, les protéines comme TGF-beta1, TFG-beta2, BMP2/4 et TNF-alpha engendrent la phase catagène.
Les facteurs de croissance IGF-1 (Insulin-like Growth Factor One), les hépatocytes HGF, les facteurs de croissance VEGF de l’endothélium vasculaire (Vascular Endothelial Growth Factor) et les facteurs de croissance de type FGF participent au prolongement de la phase anagène.
Une autre molécule qui contrôle les transitions entre les phases anagène et catagène sont les récepteurs de la vitamine D.
La phase télogène coïncide avec de grands changements dans les activités des gènes. En effet, certaines protéines régulatrices, comme les récepteurs aux œstrogènes, sont sur-représentés pendant cette phase. La phase télogène n’est donc pas une phase complètement de repos. Elle est même peut-être une phase cruciale dans le contrôle du cycles des cheveux.
En fait, la phase télogène peut être divisée en une phase réfractaire aux stimuli qui induisent la croissance du follicule et caractérisée par la surrégulation et activation des protéines BMP2/4 et une phase complémentaire où les cellules souches du bulbe deviennent très sensibles aux facteurs induisant la phase anagène. Durant cette phase, la voie de signalisation BMP s’éteint alors que la voie de signalisation Wnt/beta-caténine s’active et atteint un niveau optimal d’activité au début de la phase anagène.
Pendant la phase télogène, on a vu que les papilles dermiques sont juste au-dessous du bulbe. Lorsqu’une concentration assez élevée d’activateurs de cellules souches est atteinte, la phase anagène reprend.
Certaines molécules qui jouent un rôle dans la balance qui fait que les cellules souches sont au repos ou non ont été identifiées. Alors que les cellules souches semblent être maintenues au repos par l’activation de la voie de signalisation BMP en combinaison avec l’inhibition de la voie Wnt par les protéines TCF3 et DKKs, elles s’activent par l’inhibition de la voie BMP et l’activation de la voie Wnt avec une stabilisation de la protéine beta-caténine :
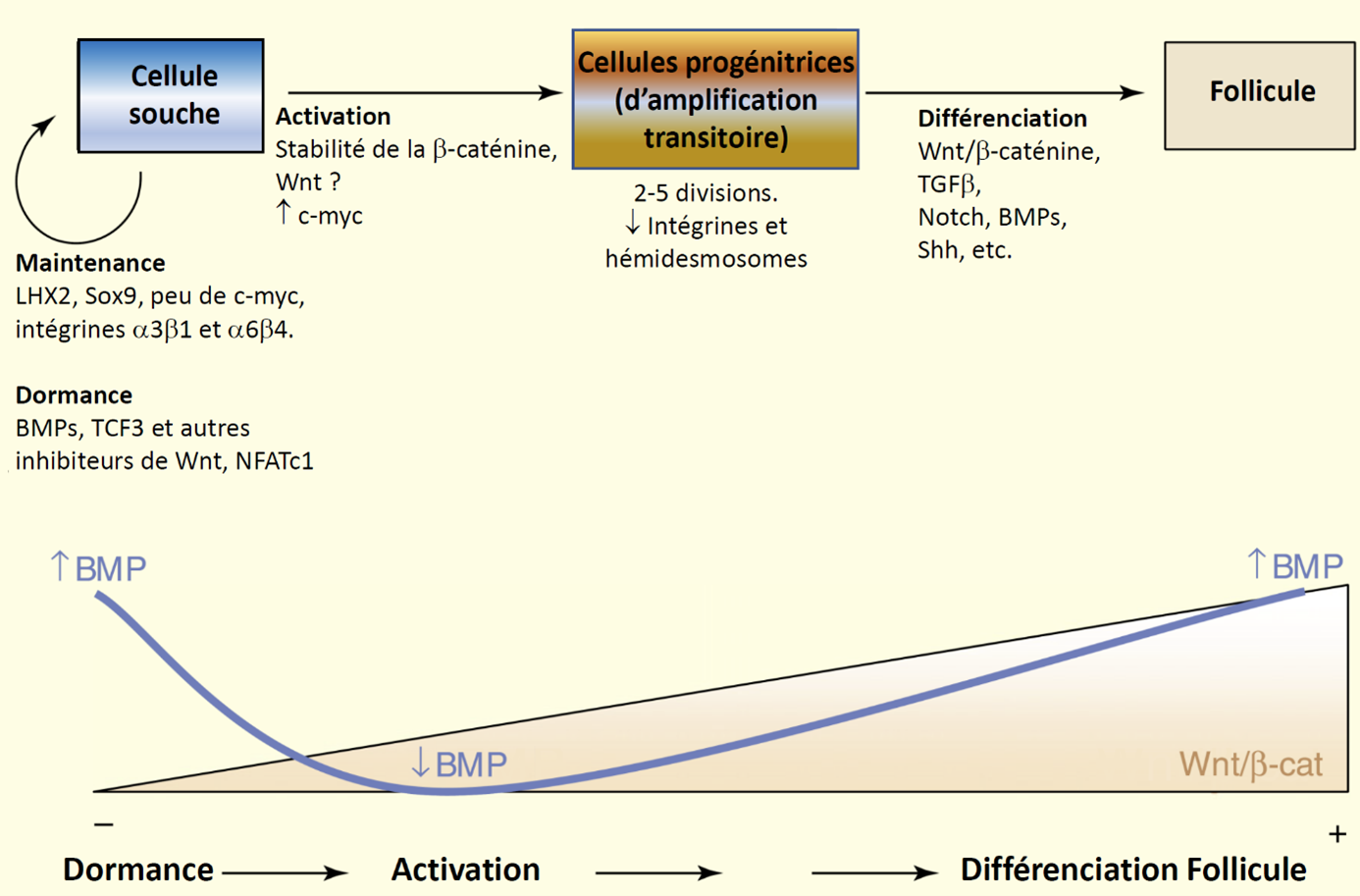
Au cours du début de la phase anagène, le bulbe s’écarte progressivement de la papille dermique et les cellules souches épithéliales entrent en dormance. Cependant, la voie de signalisation Wnt/beta-caténine demeure active grâce aux cellules progénitrices (d’amplification transitoire) contenues dans la matrice du cheveu. Ces cellules stabilisent également la beta-caténine tout au long de la phase anagène. Un peu plus haut dans la matrice ces cellules arrêtent de proliférer et initient les différenciations terminales en différentes lignées de cellules épithéliales.
De nombreuses molécules régulatrice de la formation de la gaine épithéliale interne et externes ont été découvertes. Par exemple, GATA3, Cutl1 et les BMPs participent à la formation de la gaine épithéliale interne, Sox9 et SHH participent à la formation de la gaine épithéliale externe, et Wnt/beta-caténine, les récepteurs à la vitamine D, Notch, les BMPs et Foxn1 participent à la formation de la tige du cheveu. À l’opposé, TCF3 est un inhibiteur général de l’ensemble des lignées des cellules épithéliales.
Des expériences ont montré que les exosomes MSC-ASC engendrent la croissance des cheveux
Les exosomes contiennent des micro-ARN qui, lorsque délivrés aux autres cellules, vont en affecter le comportement. Les micro-ARN contenus dans les exosomes varient en fonction des cellules souches desquelles elles proviennent. Certains micro-ARN vont accentuer la proliférations des follicules alors que d’autres auront tendance à les ralentir.
La régulation de la croissance des follicules est régulée par un mécanisme paracrine dans lesquels les exosomes des cellules des papilles dermiques jouent un rôle essentiel.
Mais en plus de ce type de cellules, des ASC localisées dans les tissus adipeux sous le derme peuvent également jouer un rôle dans le cycle des cheveux car les ASC se différentient en adipocytes matures qui entourent les cheveux pendant la transition entre la phase télogène - anagène.
De nombreuses études ont également montré que les ASC ont un effet sur la croissance des cheveux en augmentant la prolifération des cellules des papilles dermiques. Cela vient du fait que les interactions entre les cellules ASC et les cellules des papilles dermiques sont contrôlées par divers médiateurs qui active la transition télogène – anagène. En particulier, comme on l’a vu, la voie de signalisation Wnt/beta-caténine et les facteurs de croissance IFG-1 produits par les cellules des papilles dermiques. Les exosomes dérivés des cellules souches MSC véhiculent un grand nombre de facteurs de croissance et d’activateurs de la signalisation Wnt/beta-caténine.
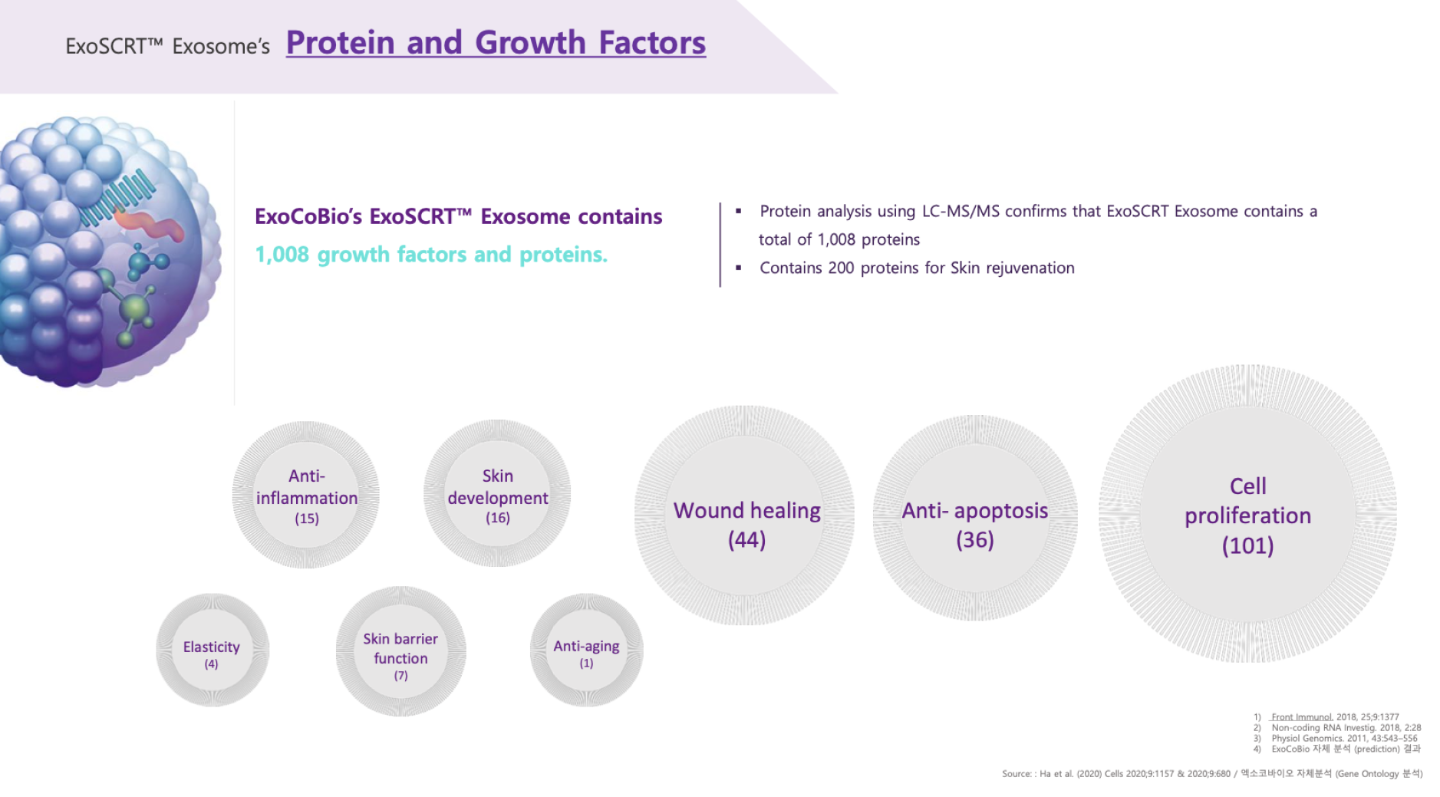
Les protéines contenues dans les exosomes du produit ASCE+ HRLV
Ci-dessous sont répertoriées certaines protéines transportées par les exosomes contenus dans le produit ASCE+ HRLV. On peut remarquer qu’un grand nombre d’entre elles participent au bon développement des follicules :
Ces deux groupes de protéines travaillent en synergie pour promouvoir la prolifération de la kératinocyte (cellules constitutives de la couche externe de la peau)
Alopécie et DHT
On a vu que la croissance des cheveux est gouvernée par divers facteurs endogènes, comme la signalisation intra-cellulaire et inter-cellulaire. Par exemple, la signalisation BMP et TGF (en particulier les facteurs TFG-beta1 et TGF-beta2) sont connues pour inhiber l’induction de la phase anagène, alors que la protéine Wnt10b stimule le passage de la phase télogène vers la phase anagène. De la même manière, les facteurs de croissance de type FGF induisent la phase anagène. Enfin, d’autres voies de signalisation, lorsqu’elles sont suractivées ou au contraire sous-activées, jouent un rôle dans le cycle des cheveux chez l’adulte :
L’une des principales conséquences de l’alopécie est la réduction progressive de la durée de la phase anagène. Les follicules passent prématurément de la phase anagène vers la phase catagène. Une autre raison la miniaturisation des cheveux, processus pendant lequel les cheveux solides terminaux sont transformés en cheveux-duvets.
L’influence de l’hormone androgène DHT (dihydrotestostérone) sur la chute des cheveux est bien connue. Les androgènes, dont la DHT, entrent dans les follicules par le réseau capillaire de la papille dermique. Ils s’accrochent ensuite aux récepteurs androgènes contenus dans les cellules de la papille dermique, et activent ou au contraire désactivent certains gènes. Or, chez les personnes atteintes d’alopécie, les cellules des papilles dermiques contenues dans les follicules secrètent les protéines TGF-beta1 et TGF-beta2. Celles-ci inhibent la croissance des cellules épithéliales en réponse aux androgènes.
Dans le corps, la testostérone est convertie en DHT par l’enzyme 5-alpha-réductase. Or, des expériences ont montré que les cellules des papilles dermiques issues des follicules de l’avant du scalp (qui contiennent moins de récepteurs coactivateurs transcriptionnels aux androgènes ARA70-beta/ELE1-beta mais davantage de récepteurs androgènes de type II 5alpha-réductase que les cellules des papilles dermiques occipitales - qui « ne tombent pas »), sont connues pour secréter des facteurs autocrines inhibants qui affectent la croissance des cellules. Cela montre bien que la DHT altère les processus autocrines et paracrines et joue un rôle essentiel dans la chute des cheveux, plus que les autres androgènes.
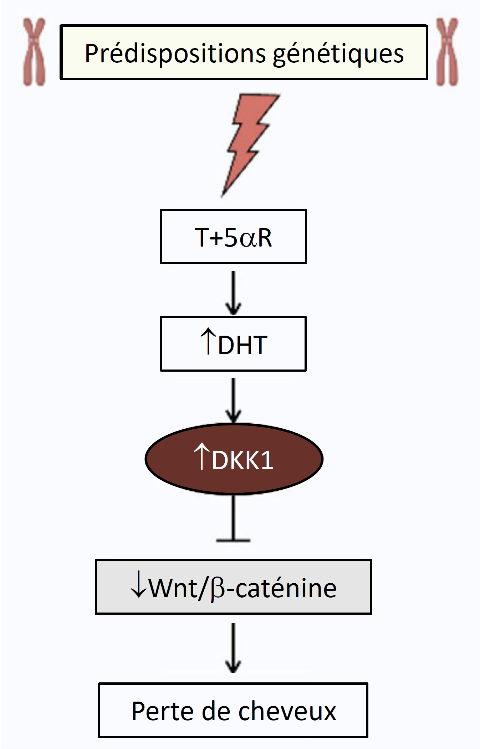
Plusieurs recherches ont montré que sous l’effet de la DHT, le gène DKK1 (dickkopf 1) est sur-régulé dans les cellules des papilles dermiques des personnes atteintes d’alopécie. Cette sur-représentation a également un impact sur la croissance des kératinocytes dans la gaine épithéliale externe.
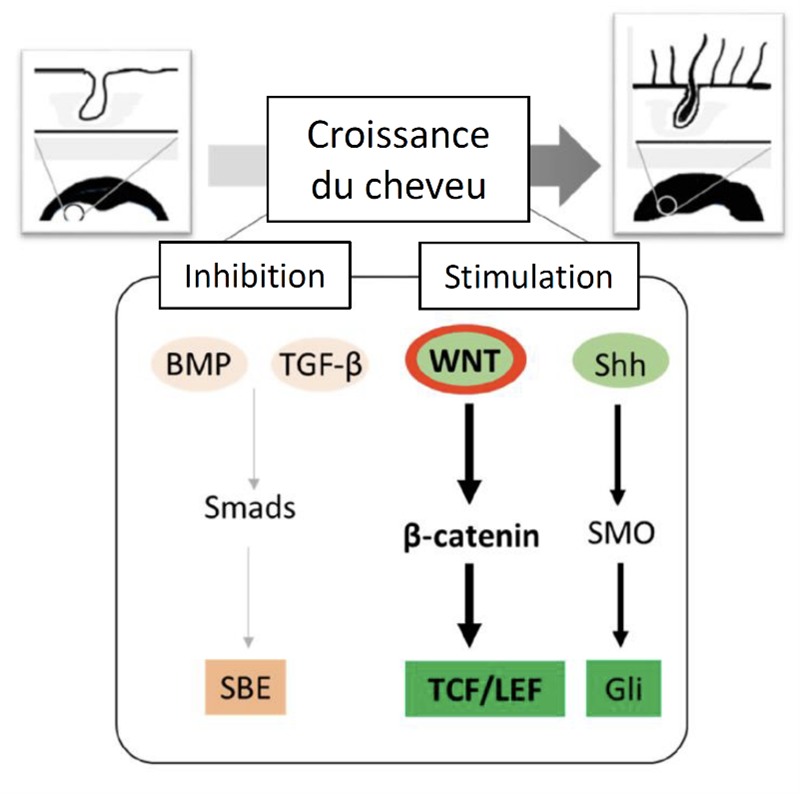
Nous allons voir dans la section suivante que la protéine Dkk1 joue un rôle très important dans l’inhibition du bon déroulement de la voie de transduction canonique Wnt/beta-caténine. Le rôle que joue la DHT sur nos cheveux peut donc être résumé par le petit schéma suivant :
L’importance de la voie de signalisation Wnt/beta-caténine sur la croissance des cheveux
On l’a vu : il y a de nombreux facteurs endogènes qui influences la croissance des cheveux, dont les molécules impliquées dans les voies de signalisations intercellulaires et extracellulaires. L’activation de la phase anagène est inhibée par l’activation des protéines de signalisation BMP et des facteurs de croissances TGF-beta. En revanche, les voies de signalisations Wnt/beta-caténine et hedgehog (SHH) stimulent la croissance des cheveux et l’entrée en phase anagène.
On va voir que dans le cas de la voie de signalisation Wnt engendrant la croissance des cheveux, la protéine beta-caténine est stabilisée dans le cytoplasme de la cellule et transloquée dans le noyau, où elle agit avec des protéines de la famille TCF/LEF comme facteur de transcription. Dans ce cas, on dit que la voie Wnt est canonique. Il en résulte l’activation de gènes qui promeuvent l’activation de la phase anagène et donc de la croissance d’un nouveau cheveu.
La famille TCF/LEF (T-cell factor / Lymphoid Enchancer Factor) est un groupe de gènes qui encodent des facteurs de transcription. Ils interviennent dans la voie de signalisation Wnt, en particulier pendant la phase embryonnaire et le développement des cellules souches, mais ils jouent également un rôle dans le cancer et le diabète. Les facteurs TCF/LEF recrutent la beta-caténine comme coactivateur afin d’augmenter la probabilité de transcription d’un gène spécifique. Ils peuvent également au contraire recruter un membre de la famille Groucho comme corépresseurs (et donc diminuer la probabilité de transcription des gènes). Lorsque la protéine betya-caténine n’est pas transloquée dans le noyau mais détruite dans le cytoplasme de la cellule, c’est la protéine de la famille Groucho qui est recrutée par les facteurs TCF/LEF. Dans ce cas, on dit que la voie de signalisation n’est pas canonique. C’est ce qui se passe malheureusement chez les personnes atteintes d’alopécie.
De nombreuses recherches ont montré que de multiples protéines de la famille Wnt interviennent dans le bon déroulement du cycle du cheveu et de sa régénération. Par exemple :
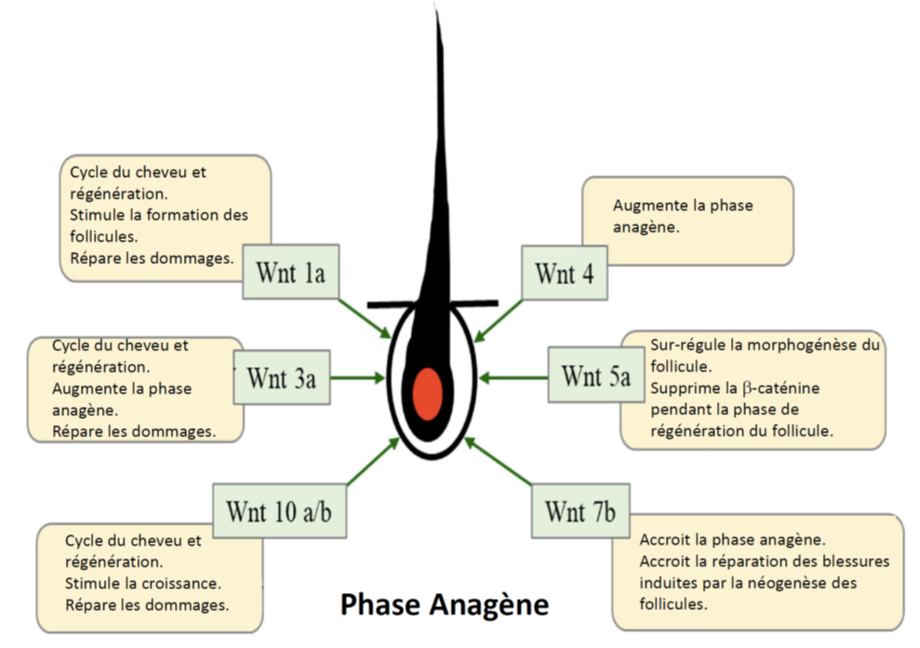
Parmi l’ensemble des voies de signalisation associées dans le cycle des cheveux, de nombreuses études assument que celle de le Wnt/beta-caténine est la plus importante parce que la DHT, qui est sur-régulée dans l’alopécie, altère cette voie de signalisation. Les principaux inhibiteurs de cette voie de signalisation sont les protéines DKK1, SFRP2 (Secreted Frizzled-Related Protein 2) de la famille SFRP et la sclérotine (qui se fixe sur BMP7).
La DKK1 est un puissant inhibiteur de la voie de transduction Wnt/beta-caténine et des expériences ont montré que des injections de DKK1 dans le scalp de souris active la transition anagène – catagène. Cette protéine est sur-représentée chez les patients atteints d’alopécie et la DHT interfère le cycle normal du cheveu de manière négative en activant la phase catagène par implication de la DKK1.
Il est donc raisonnable de postuler que l’inhibition de la DKK1 est une clé pour promouvoir la croissance des cheveux chez les personnes atteintes d’alopécie. De plus, il existe un certain nombre de micro-ARN qui ciblent la DKK1 et sont impliqués dans les voies de signalisation en rapport à la croissance des cheveux.
Voyons maintenant plus en détails comment fonctionne la voie de signalisation canonique Wnt/beta-caténine et comment celle-ci est détériorée dans l’alopécie.
La voie de signalisation canonique Wnt et sa détérioration dans l’alopécie
Comme déjà évoqué, la voie de signalisation canonique Wnt (ou voie de signalisation Wnt/beta-caténine) est la voie de signalisation Wnt qui provoque une accumulation de la protéine beta-caténine dans le cytoplasme de la cellule et son éventuelle translocation dans le noyau pour agir comme coactivateur transcriptionnel de facteurs de transcription appartenant à la famille TCF/LEF.Voyons plus en détails comment la protéine DKK1 influence de manière négative cette voie de signalisation canonique.
Au repos, dans le cytoplasme de la cellule se trouve de la beta-caténine qui est phosphorylée pour ne pas s’accumuler (le processus de phosphorylation est une modification chimique qui consiste à ajouter un groupement phosphate sur une molécule). Le complexe de destruction responsable de ce processus de phosphorylation est composé des protéines APC (Adenomatous Polyposis Coli), GSK-3alpha (Glycogen Synthase Kinase 3alpha), CK1alpha (Casein Kinase 1alpha) et de PP2A (Protein Phosphate 2A). Ce complexe de destruction marque la beta-caténine pour la dégradation par le protéasome (les protéasomes sont des complexes enzymatiques qui se trouvent dans le noyau des cellules et dont le rôle est de dégrader les protéines mal repliée – c’est-à-dire une protéine mal formée).
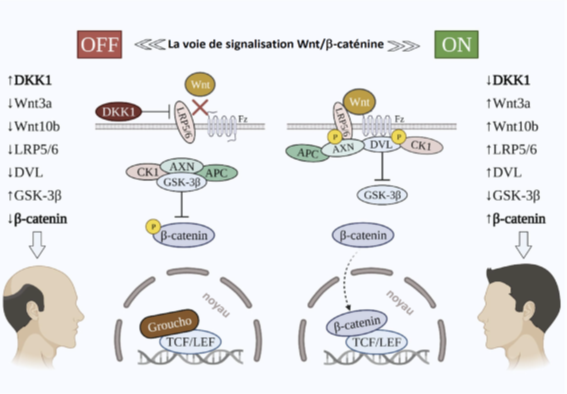
Lors de la phase canonique de la voie de signalisation Wnt/beta-caténine, les ligands Wnt s’accrochent au récepteur FZD (Frizzled) et au corécepteur LRP5/P6. Ce corécepteur est transmembranaire : une partie se trouve en dehors de la cellule et une autre dans le cytoplasme de la cellule. Dès que Wnt se lie à Frizzled et à LRP5/P6, cela provoque la translocation du régulateur Wnt négatif AXN (Axine) qui vient se lier à la queue de la protéine LRP5/P6 qui se trouve dans le cytoplasme. Le groupement de phosphate PP2A du complexe de destruction induit alors la phosphorylation de la queue de la protéine LRP5/P6. Ce processus est suivi du recrutement par phosphorylation de la phosphoprotéine DVL (dishevelled) qui vient se lier au récepteur frizzled dans l’endodomaine de la cellule ce qui inhibe l’activité de GSK-3alpha et donc désactive le complexe de destruction. Cela empêche la protéine beta-caténine d’être dégradée et d’être envoyée au protéasome pour y être digérée. La beta-caténine peut alors s’accumuler et se transloquer dans le noyau, puis se lier aux facteurs de transcription TCF/LEF. Un complexe transcriptionnel est alors formé, et la transcription d’un certain nombre de gènes de type Wnt est alors activée.
De l’autre côté, lorsque les ligands Wnt ne viennent pas se lier au récepteur FZD, la beta-caténine devient instable dans le cytoplasme car elle est phosphorylée par GSK-3alpha et CK1 puisque le régulateur négatif AXN n’est pas transloqué au niveau de la queue de LRP5/P6, et donc DVL n’est pas recruté. La GSK-3alpha n’est alors pas inhibée et le complexe transcriptionnel n’est donc pas formé dans le noyau. Dans ce cas, le facteur de transcription TCF/LEF recrute un membre de la famille Groucho comme corépresseur.
Des études ont montré que lorsque les protéines DKK1 sont sur-régulées, elles se lient à LRP5/P6, ce qui supprime la cascade de signalisation de Wnt, et inhibe le développement des follicules, et donc la croissance des cheveux. La protéine DKK1 est donc un facteur clé dans le développement de l’alopécie.
Certaines études semblent montrer également que la protéine SFRP2 pourrait inhiber la voie de signalisation Wnt/beta-caténine, mais cela n’est pas encore avéré. En effet, un traitement avec des recombinants humains de SFRP2 sur des cellules de papilles dermiques extraites de patients se faisant greffer a considérablement augmenté la signalisation Wnt canonique.
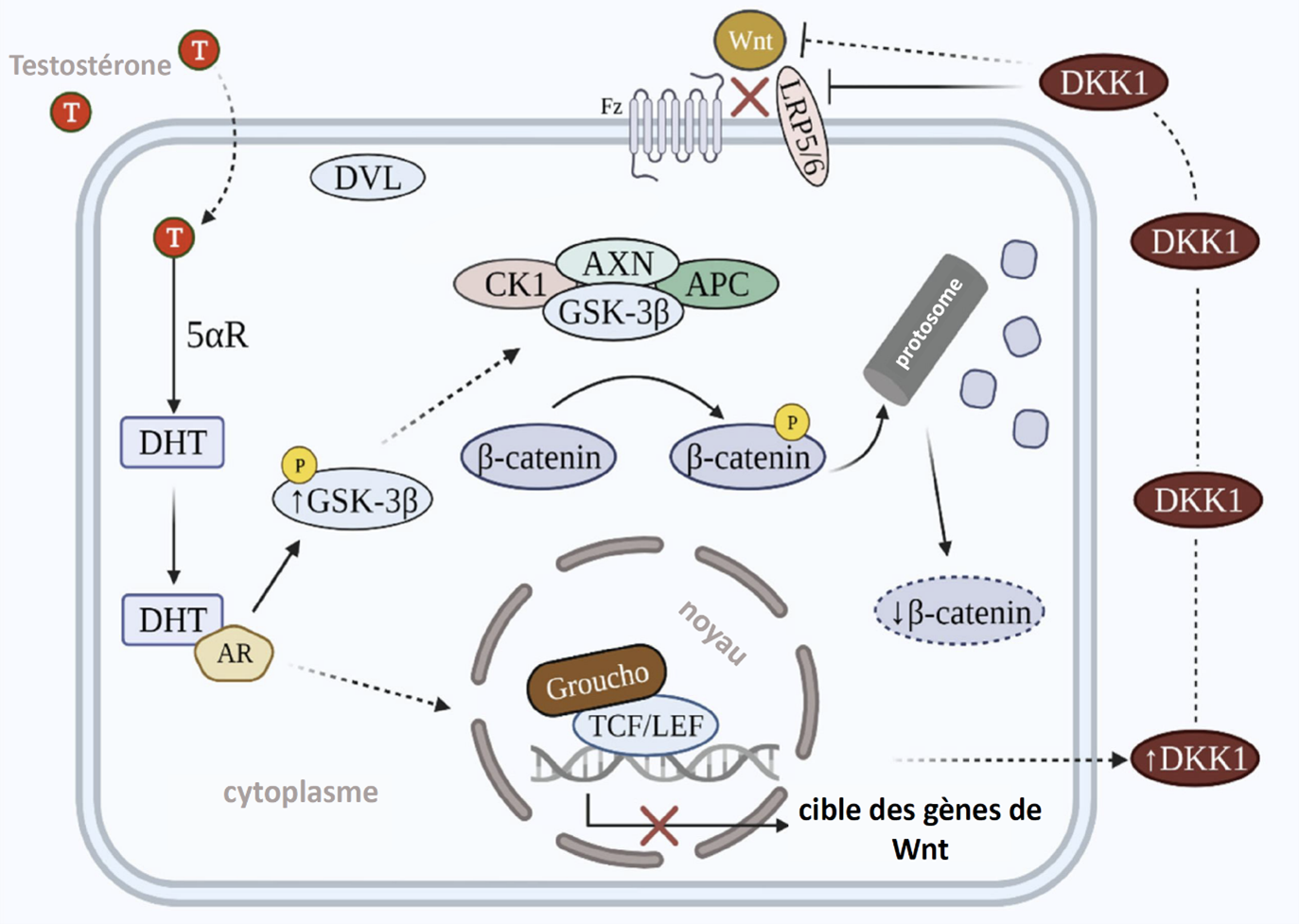
De quelle manière la DHT induit-elle la DKK1
Les études ont montré que le niveau de DHT et de DKK1 sont corrélés. Dans le corps, la 5 alpha-réductase (5alphaR) convertit la testostérone en DHT. Cette hormone androgène joue un rôle inhibiteur sur la croissance des cellules de la gaine épithéliale externe ce qui induit une perturbation sur la croissance normale des cheveux. Des expériences ont également montré que les anti DKK1 diminuent fortement l’inhibition de la croissance des cellules de la gaine épithéliale externe. De plus, la concentration de DKK1 est supérieure dans le scalp des personnes atteintes d’alopécie. Enfin, des études ont montré que la DKK1 perturbée par la DHT stimule l’apoptose des cellules kératinocytes.
Quelques sont les molécules qui inhibent la protéine DKK1
Quelques études se sont intéressées de l’effet de certaines molécules sur la voie Wnt canonique. Une étude a observé l’impact de la morroniside, une molécule naturelle qui se trouve dans le Cornouiller mâle (parfois appelé cornier ou fuselier), sur la voie de signalisation Wnt canonique dans les cellules de la gaine épithéliale externe. Les résultats montrent une augmentation de la prolifération des cellules ainsi qu’une augmentation de la beta-caténine. Une autre étude concomitante a montré que ce traitement a agi sur la DKK1.
Un autre composé naturel, la vitexine (qui se trouve par exemple dans la Passiflore), permet d’augmenter de manière significative la prolifération les papilles dermiques dans les follicules. Là encore, il a été montré la vitexine sur-régule la beta-caténine et diminue de manière substantielle le niveau de DKK1.
L’extrait de Ginseg a également engendré une prolifération des kératinocytes dans la gaine épithéliale externe, l’inhibition de l’apoptose, et a révélé l’effet de DKK1.
Un autre composé naturel qui active la voie Wnt/beta-caténine et SHH tout en inhibant les voies TGF-beta/SMAD et BMP dans les follicules, et induit par conséquent la croissance des cheveux, est le costunolide. On le trouve dans le costus indien.
Les composants essentiels du Ginkgo bilboa, le Ginkolide B et la Bilobalide, sont également connus comme des molécules pouvant aider à la croissance des cheveux. Ces molécules sont associées à l’activation de la voie Wnt/beta-caténine via l’inhibition de l’expression des gènes DKK1.
L’antidépresseur tianeptine est connu pour avoir un impact sur le diamètre des cheveux, et donc la croissance des cheveux, par inhibition de DKK1. Il ralentit également la transition de la phase anagène vers la phase catagène chez les personnes atteintes d’alopécie.
Enfin, le minoxidil sous-régule également la production de DKK1 et de TGF-beta dans les cellules kératinocytes.
On voit donc que beaucoup d’études montrent l’influence de l’inhibition de la DKK1 dans la croissance des cheveux.
Le rôle des micro-ARN pour moduler la croissance des cheveux
Un certain nombre de micro-ARN sont impliqués dans la croissance des cheveux et la déficience de la voie Wnt canonique impacte cette croissance. L’idée est donc d’utiliser certains micro-ARN pour réguler cette voie. Je me suis précédemment concentré dans ce rapport sur l’étude de la voie Wnt qui est la voie la plus importante dans le domaine de la croissance des cheveux, mais comme nous l’avons déjà évoqué précédemment, de nombreuses autres voies de signalisation interviennent dans le processus de croissance des cheveux.
Dans ce qui suit, je me suis penché en particulier sur les micro-ARN que l’on trouve dans les exosomes de cellules souches MSC et issues de papilles dermique.
Une étude a montré que des exosomes issues de cellules de papilles dermiques contiennent près de 200 micro-ARN. Les 34 micro-ARN sur-représentés ou au contraire sous-représentés sont les suivants : let-7b-5p, let-7c-5p, let-7f-5p, let-7g-5p, miR-1, miR-103-3p, miR-122, miR-126-3p, miR-126-5p, miR-128-3p, miR-133a-3p, miR-145-5p, miR-148b-3p, miR-193b-5p, miR-199c-3p, miR-199c-5p, miR-200a, miR-200c, miR-214-3p, miR-222-3p, miR-22-5p, miR-24-3p, miR-27b-3p, miR-320-3p, miR-330-5p, miR-3432-5p, miR-34a, miR-423-5p, miR-449a-5p, miR-451-5p, miR-499-5p, et miR-99a-5p.
Cette étude a montré que ces micro-ARN sont impliqués dans 40 fonctions biologiques, en particulier dans celles en lien avec la communication intercellulaires intervenant dans les follicules comme :
Ces 34 micro-ARN ciblent potentiellement 33 055 gènes. L’expression de certain de ces gènes aura comme conséquence d’accroitre ou de diminuer le nombre de protéines codées. Ainsi, certains micro-ARN ont un effet positif sur la croissance des cheveux alors que d’autres auront un effet négatif.Cette même étude a ensuite étudié l’interaction de ces 34 micro-ARN avec 29 gènes impliqués dans la croissance des cheveux afin d’identifier les micro-ARN les plus représentés :
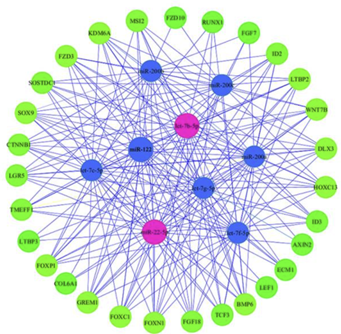
Les 9 représentants sont les micro-ARN miR-200b, miR-200c, let-7b-5p, miR-122, miR-200a, let-7g-5p, let-7c-5p, miR-22-5p, et let-7f-5p. Parmi eux, les micro-ARN principaux identifiés comme ciblant les gènes en relation avec la croissance des follicules sont miR-22-5p et let-7b-5p. L’étude a ensuite montré expérimentalement que miR-22-5p inhibe la prolifération des cellules souches des follicules en ciblant le gène LEF1, impliqué dans la voie canonique Wnt.
Bien entendu, d’autres micro-ARN issus éventuellement d’autres exosomes provenant de cellules souches différentes peuvent avoir un impact sur le développement des cheveux. On sait que les exosomes issues de cellules souches MSC ont un effets bénéfique sur la croissance des cheveux. On y trouve les micro-ARN suivants :
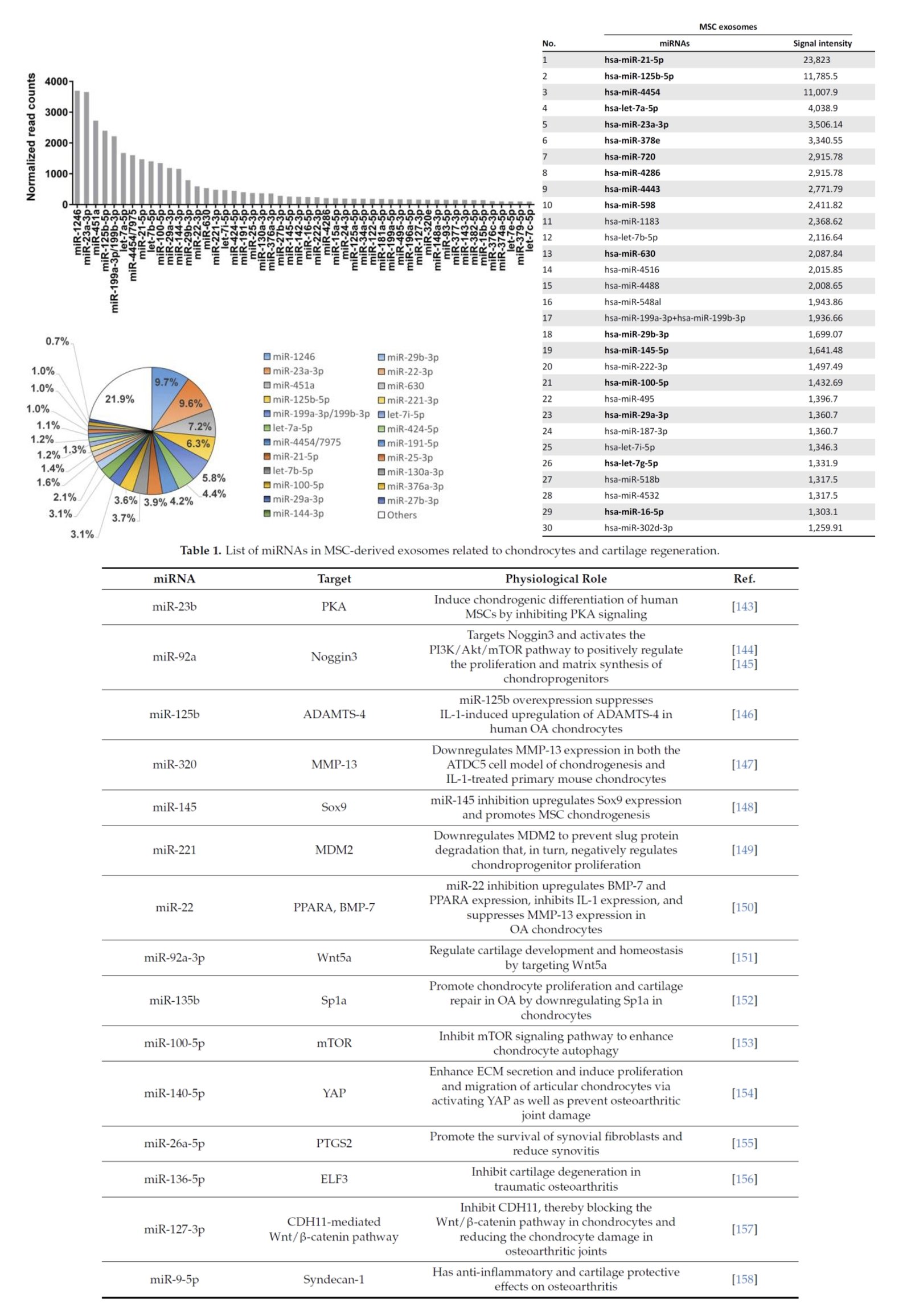
On sait également que les exosomes issues de cellules souches MSC-ASC ont un effets bénéfique sur la croissance des cheveux. On y trouve les 50 micro-ARN les plus représentés suivants :
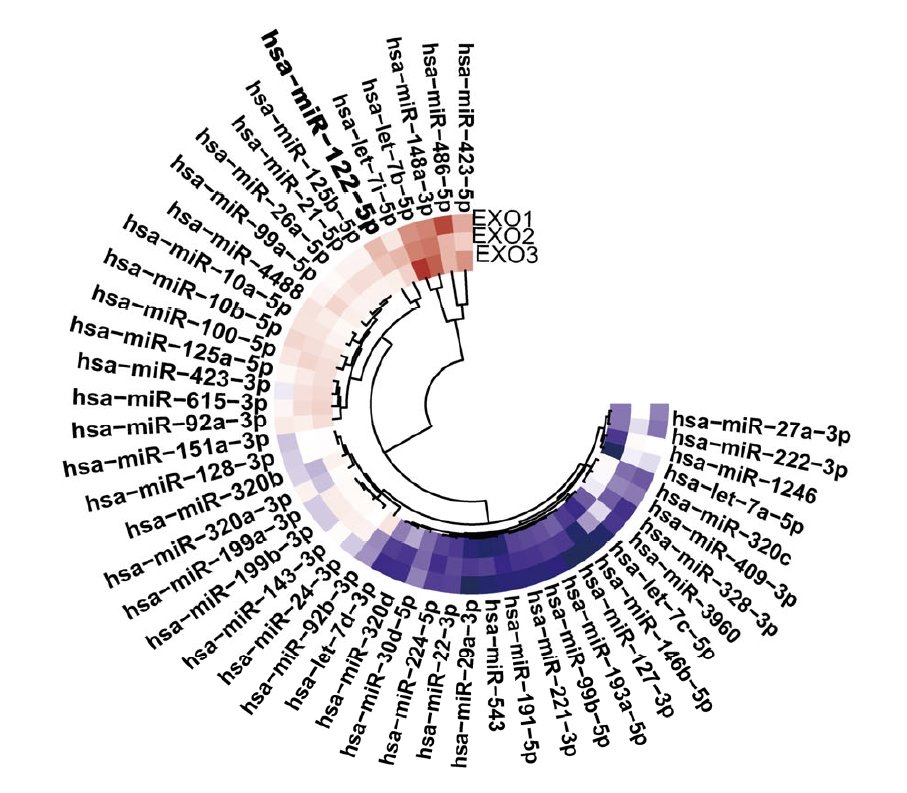
Les 5 micro-ARN les plus représentés dans les exosomes MSC-ASC sont les suivants :

Parmi les micro-ARN ayant un impact sur la régulation de la DKK1, on retrouve par exemple :
Parmi les micro-ARN connus pour avoir un impact sur la croissance des cheveux on trouve par exemple :
Il est intéressant de noter que même la présence de micro-ARN qui jouent un rôle négatif sur la croissance des cheveux de manière indépendante (comme miR-22 dans les exosomes MSC) n’empêchent pas les exosomes de ces cellules souches d’avoir dans l’ensemble une action positive. Je pense que cela vient du fait que leur nombre est inférieur en proportion aux autres micro-ARN qui ont une action positive et que la dynamique sur laquelle jouent l’ensemble des micro-ARN est très complexe. Des phénomènes de compensation doivent certainement intervenir.
Quels sont les micro-ARN contenus dans les exosomes ASCE+ HRLV ?
La question est donc de savoir si les micro-ARN contenus dans le produit ASCE+ HRLV peuvent jouer un rôle bénéfique sur la prolifération des follicules, leur maintien en phase anagène, ou encore la capacité de forcer les cheveux à passer rapidement de la phase télogène vers la phase anagène.
Malheureusement, les exosomes contenues dans le produit ASCE+ HRLV ne sont pas des exosomes extraites de cellules souches des papilles dermiques, ni des cellules souches mésenchymateuse. La raison est qu’il est interdit de vendre au grand public de telles exosomes dans certains pays (comme en Europe, au royaume unis, aux US, …), alors que cela peut se faire dans d’autres pays (Corée, Japon, …).
Les exosomes contenues dans le produit ASCE+ HRLV proviennent de cellules souches de rose (le terme anglais est « Rose stem cell exosomes »). La société ExoCoBio a déposé en particulier le brevet « ExoSCRT » permettant cette extraction. Cela permet de rendre accessible l’utilisation de dérivés des exosomes MSC dans certains pays où les exosomes issues de cellules souches humaine sont interdites. Ces exosomes possèdent des propriétés de synthétisation du collagène et des propriétés anti-inflammatoires.
L’étude de ces exosomes a montré qu’elles partagent 904 micro-ARN avec ceux que l’on trouve chez les humains. Parmi ces micro-RNA, 5 sont en relation directe avec la prolifération des cellules et trois (miR-8485, miR-574-5p et mir-1246) jouent un rôle dans la régulation de la signalisation Wnt :

Parmi les micro-ARN identifiés comme ayant un impact sur la croissance des cheveux, on trouve un certain nombre qui sont interessants :
Parmi ceux que l’on trouve également dans les exosomes MSC ou des extraits des cellules souches des papilles dermiques, on trouve : miR-let-7a-5p, miR-let-7b-5p, miR-let-7c-5p, miR-let-7f-5p, miR-let-7g-5p, miR-let-7i-5p, miR-1-3p, miR-122-5p, miR-1246, miR-130a-3p, miR-21-5p, miR-214-3p, miR-23a-3p, miR-23b-3p, miR-29b-3p, miR-4488.
De nombreux micro-ARN transportés dans les exosomes de rose ont également des effets anti-âge, anti-inflammatoires et des propriétés régénératrices et de cicatrisation des plaies. Je n’ai pas étudié ces micro-ARN car je me suis concentré sur ceux qui ont un impact sur les cheveux, mais voici la synthèse donnée par le laboratoire ExoCoBio sur les exosomes ASCE+ HRLV :
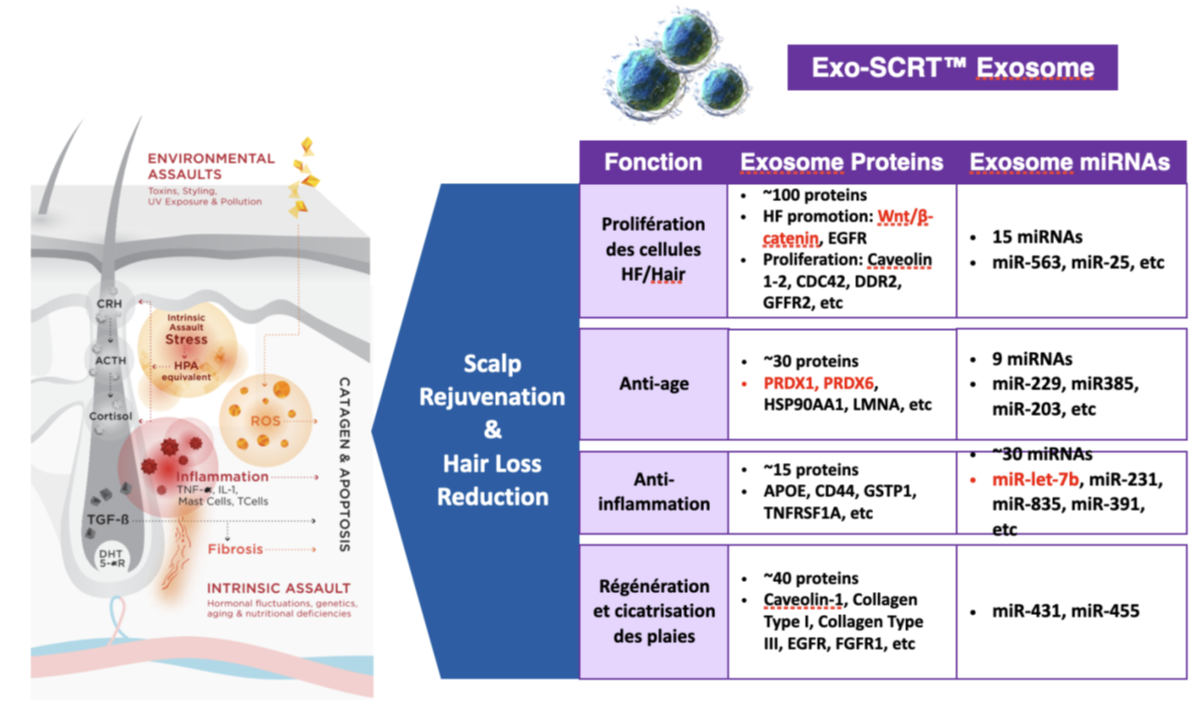
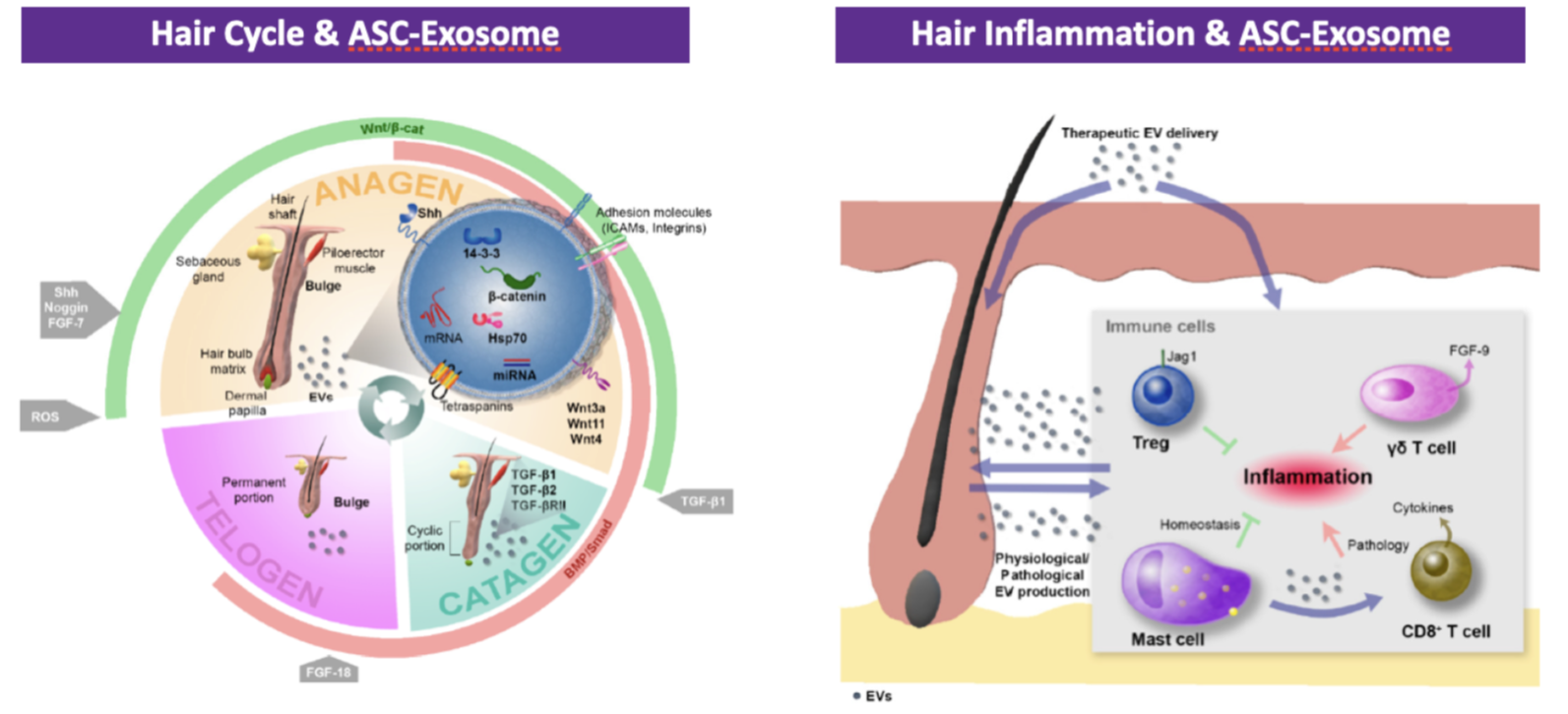

Les autres ingrédients contenus dans le produit ASCE+ HRLV

Le produit ASCE+ HRLV semble donc intéressant car il contient beaucoup de facteurs de croissances et de micro-ARN qui possèdent des actions positives sur la croissance des cheveux.Cependant quelques questions subsistent :
Je n’ai pas pu trouver la liste complète des micro-ARN contenus dans les exosomes de rose mais les données devraient normalement être publiques prochainement. Cela serait intéressant de savoir si d’autres micro-ARN avec une action négative ou positives sont contenus dans ces exosomes.Voilà j’espère que ce petit rapport sur les exosomes vous aura intéressé et que vous aurez (comme moi) appris des trucs !
N'hésitez pas à me contacter sur le forum https://www.hairrestorationnetwork.com (mon pseudo est arthurSam) : Cliquez ici pour m'envoyer un message !